题目内容
【题目】下列装置能达到实验目的的是( )
A.制备乙烯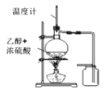
B.除去甲烷中少量的乙烯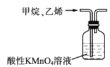
C.从碘的苯溶液中分离碘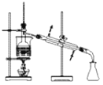
D.验证乙炔的还原性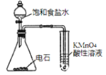
【答案】C
【解析】
A选项,制备乙烯温度计测定的是溶液的温度,温度计要在液面以下,乙烯密度与空气相接近,用排水法收集,故A错误,不符合题意;
B选项,除去甲烷中少量的乙烯,乙烯会被高锰酸钾氧化成二氧化碳气体,生成新的杂质气体,不能达到除杂目的,故B错误,不符合题意;
C选项,从碘的苯溶液中分离碘采用蒸馏的方法,图示蒸馏操作正确,故C正确,符合题意;
D选项,电石和水反应除了生成乙炔还会生成少量的硫化氢、磷化氢等杂质气体,杂质气体能使高锰酸钾褪色,如此不能验证乙炔的还原性,故D错误,不符合题意。
综上所述,答案为C。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】为提纯下列物质![]() 括号内为杂质
括号内为杂质![]() ,所用的除杂试剂和分离方法都正确的是( )
,所用的除杂试剂和分离方法都正确的是( )
序号 | 不纯物 | 除杂试剂 | 分离方法 |
A | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
B | 溴乙烷(Br2) | NaOH溶液 | 蒸馏 |
C | 溴苯(液溴) | 乙醇 | 分液 |
D | 乙醇(水) | 新制生石灰 | 蒸馏 |
A.AB.BC.CD.D
【题目】某校化学兴趣小组的同学用滴定法对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,回答下列问题:
(1)用分析天平准确称取该样品5.0g,全部溶于水配制成1000.0mL的溶液。用____(填一仪器名称)量取其中20.00mL放在锥形瓶中,滴加几滴指示剂,待测。该中和滴定中可选用的指示剂是__________________________,(如有几种,可任填一种)滴定终点的现象是___________________________________________________________。
(2)用0.10mol/L的盐酸溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,
实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
1 | 20.00 | 24.01 |
2 | 20.00 | 23.99 |
3 | 20.00 | 22.10 |
计算样品中,NaOH的质量百分含量为__________________。
(3)若滴定前,滴定管尖端有气泡,滴定终了气泡消失,将使所测结果______(填“偏高”、“偏低”或“不变”,下同),若读酸式滴定管读数时,滴定前仰视读数,滴定后正确读数,则所测结果_______;
(4)下图为0.10mol/L 25 mL NaOH溶液中逐滴滴加0.10mol/L CH3COOH溶液过程中溶液pH的变化曲线,请回答:
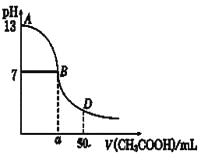
①B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?______(选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?________区间。(若正确,此问不答)。
②在D点时,溶液中c(CH3COO-)+c(CH3COOH)______2c(Na+)。(填“>”、“<”或“=”)