题目内容
【题目】下列离子方程式正确的是( )
A.碳酸钡溶于盐酸溶液中:BaCO3+2H+===Ba2++H2O+CO2↑
B.小苏打溶液与氢氧化钠溶液混合:![]() +OH-===CO2↑+H2O
+OH-===CO2↑+H2O
C.氯化钙溶液与碳酸氢钾溶液混合:Ca2++![]() ===CaCO3↓
===CaCO3↓
D.硫酸铜溶液与氢氧化钡溶液混合:![]() + Ba2+===BaSO4↓
+ Ba2+===BaSO4↓
【答案】A
【解析】
A.碳酸钡与盐酸反应的离子反应为:2H++BaCO3=Ba2++H2O+CO2↑,故A正确;
B.小苏打溶液与氢氧化钠溶液混合反应的离子反应为:HCO3-+OH-=CO32-+H2O,B错误;
C.氯化钙溶液与碳酸氢钾溶液混合不发生反应,C错误;
D.硫酸铜溶液与氢氧化钡溶液混合反应的离子反应为:Cu2++SO42-+ Ba2++2OH- = Cu(OH)2↓+2H2O,D错误;
答案选A。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
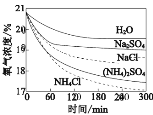
【题目】利用如下实验探究铁钉在不同溶液中的吸氧腐蚀。
实验装置 | 实验编 号 | 浸泡液 | pH | 氧气浓度随时间的变化 |
| ① | H2O | 7 |
|
② | 1.0 mol·L-1 NH4Cl | 5 | ||
③ | 0.5 mol·L-1 (NH4)2SO4 | 5 | ||
④ | 1.0 mol·L-1 NaCl | 7 | ||
⑤ | 0.5 mol·L-1Na2SO4 | 7 |
下列说法不正确的是
A.①与④⑤比较说明盐溶液可以加快吸氧腐蚀速率
B.向实验②溶液中加等体积的 0.5 mol·L-1 (NH4)2SO4,吸氧腐蚀速率一定加快
C.②与③、④与⑤比较说明吸氧腐蚀速率可能与阴离子种类有关
D.向实验⑤溶液中加入少量(NH4)2SO4 固体,吸氧腐蚀速率加快