题目内容
6.(s已知在25℃时:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1=-890.3J•mol-,C(石墨)+O2(g)=CO2(g)△H2=-393.5kJ•mol-1 H2(g)+$\frac{1}{2}$O2(g)=H2O(l);△H=-285.8kJ•mol-则由石墨生成甲烷的反应热△H为:C石墨)+2H2(g)=CH4(g)△H=( )| A. | -74.8kJ.mol-1 | B. | +74.8kJ.mol-1 | C. | -149.6kJ.mol-1 | D. | +149.6kJ.mol-1 |
分析 根据盖斯定律,由已知热化学方程式乘以合适的系数进行加减构造目标目标热化学方程式,反应热也乘以相应的系数,进行相应的加减,据此计算;
解答 解:已知:①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ•mol-1
②C(石墨)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
③2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1
根据盖斯定律,得②+③-①得C(石墨)+2H2(g)=CH4(g),故△H=(-393.5kJ•mol-1)+(-571.6kJ•mol-1)-(-890.3kJ•mol-1)=-74.8kJ•mol-1;
故选A.
点评 本题考查反应热的有关计算,难度中等,注意掌握盖斯定律的运用.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
17.下列有关化学键的叙述,正确的是( )
| A. | 硫酸氢钠溶于水既有离子键被破坏又有共价键被破坏 | |
| B. | 单质分子中均含共价键 | |
| C. | HF与HBr相比,分子内共价键更强,所以HF沸点更高 | |
| D. | 由不同元素组成的多原子分子里,只存在极性键 |
14.某温度下,在体积一定的密闭容器中投入反应物达到平衡,已知反应方程式为mX(g)+nY(g)?qZ(g)△H>0,m+n>q,下列叙述正确的是( )
| A. | 通惰性气体增大压强,平衡正向移动 | |
| B. | 再加入X,反应吸收的热量增大 | |
| C. | 增加Y的物质的量,X的转化率减小 | |
| D. | 降低温度,c(Y):c(Z)的值变小 |
1.下表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO气体 | CO2 | 通过足量氢氧化钠溶液,并干燥 |
| B | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| C | CaO固体 | CaCO3 | 加水溶解,过滤 |
| D | FeSO4溶液 | CuSO4 | 加入足量锌粒,充分反应,过滤 |
| A. | A | B. | B | C. | C | D. | D |
11.在密闭容器中的一定量混和气体发生反应:mA(g)+nB(g)?pC(g),平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积缩小到原来的1/2时,达到新的平衡时,测得A的浓度为0.8mol/L.下列有关判断正确的是( )
| A. | m+n<p | B. | C的体积分数下降 | ||
| C. | 平衡向逆反应反向移动 | D. | A的转化率变大 |
18.在某无色透明的酸性溶液中,能共存的离子组是( )
| A. | Na+ K+ SO42- HCO3- | B. | Cu2+ K+ SO42- NO3- | ||
| C. | Na+ K+Cl- NO3- | D. | Fe3+ K+ SO42- Cl- |
15.下表列出了一些反应在使用催化剂前后的活化能的数据以及化学反应速率常数之比.
请根据表中数据分析:催化剂能加快化学反应速率(“加快”或“减小’),催化剂是通过参与反应改变反应历程,不能来提高化学反应的平衡常数,不能改变平衡转换率.
| 化学反应 | 催化剂 | Ea/KJ•mol-1 | k(催)/k(无) | |
| 无催化剂 | 有催化剂 | |||
| C12H22O11(蔗糖)+H2O═ C6H12O6 (葡萄糖)+C6H12O6(果糖) | 蔗糖酶 | 107 | 36 | 9.2×1011(310K) |
| 2HI═H2+I2 | 金 | 184 | 105 | 1.6×108(503K) |
| CH3CHO═CH4+CO | 碘 | 210 | 136 | 7.5×104(793K) |
| 2H2O2═2H2O+O2 | 过氧化氢酶 | 75 | 25 | 5.8×108(298K) |

 、
、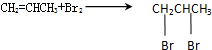 .
.