题目内容
【题目】下列事实不能用勒夏特列原理解释的是 ( )
A.氯水中存在Cl2+H2O![]() H++Cl-+HClO,当加入AgNO3溶液后,溶液颜色变浅
H++Cl-+HClO,当加入AgNO3溶液后,溶液颜色变浅
B.分别用等体积的蒸馏水和0.010mol/L硫酸洗涤BaSO4沉淀,后者损失的BaSO4沉淀少
C.SO2催化氧化成SO3的反应,往往需要使用催化剂
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
【答案】C
【解析】
A.氯水中存在Cl2+H2O![]() H++Cl-+HClO,当加入AgNO3溶液后,Ag+与溶液中的Cl-反应产生AgCl产生沉淀,使化学平衡正向移动,导致c(Cl2)降低,溶液颜色变浅,与平衡有关,A不符合题意;
H++Cl-+HClO,当加入AgNO3溶液后,Ag+与溶液中的Cl-反应产生AgCl产生沉淀,使化学平衡正向移动,导致c(Cl2)降低,溶液颜色变浅,与平衡有关,A不符合题意;
B.分别用等体积的蒸馏水和0.010mol/L硫酸洗涤BaSO4沉淀,由于BaSO4在溶液中存在沉淀溶解平衡:BaSO4(s)![]() Ba2+(aq)+SO42-(aq),用硫酸洗涤,增大了溶液中c(SO42-),溶解平衡逆向移动,因而减少了BaSO4沉淀的溶解,与平衡有关,B不符合题意;
Ba2+(aq)+SO42-(aq),用硫酸洗涤,增大了溶液中c(SO42-),溶解平衡逆向移动,因而减少了BaSO4沉淀的溶解,与平衡有关,B不符合题意;
C.SO2催化氧化成SO3的反应,往往需要使用催化剂,可以提高反应速率,而不影响化学平衡,因此对化学平衡移动无影响,C符合题意;
D.SO2与O2反应产生SO3的反应是可逆反应,增大O2的浓度,平衡正向移动,SO2转化率增大,由于开始投入量不变,因此SO2转化率增大,故与化学平衡移动有关,D不符合题意;
故合理选项是C。

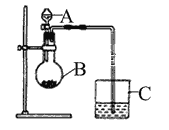
【题目】某小组通过实验研究Na2O2与水的反应。
操作 | 现象 |
向盛有4gNa2O2的烧杯中加入50mL蒸馏水得到溶液a | 剧列反应,产生能使带火星木条复燃的气体 |
取5mL溶液a于试管中,滴入两滴酚酞 | ⅰ.溶液变红 ⅱ.10分种后溶液颜色明显变浅,稍后,溶液变为无色 |
(1)Na2O2与水反应的化学方程式___。
(2)ⅱ中溶液褪色可能是溶液a中存在较多的H2O2与酚酞发生了反应。
Ⅰ.甲同学通过实验证实了H2O2的存在:取少量溶液a,加入试剂___(填化学式),有气体产生。
Ⅱ.乙同学查阅资料获悉:用KMnO4可以测定H2O2的含量:取15.00mL溶液a,用稀H2SO4酸化,逐滴加入0.003molL-1KMnO4溶液,产生气体,溶液褪色速率开始较慢后变快,至终点时共消耗20.00mLKMnO4溶液。
请配平:___MnO4-+___H2O2+___=___Mn2++___O2↑+___H2O
②溶液a中c(H2O2)=___molL-1。
③溶液褪色速率开始较慢后变快的原因可能是___。
(3)为探究现象ⅱ产生的原因,同学们继续进行了如下实验:
Ⅲ.向H2O2溶液中滴入两滴酚酞,振荡,加入5滴0.1molL-1NaOH溶液,溶液变红又迅速变无色且产生气体,10分钟后溶液变无色。
Ⅳ.向0.1molL-1NaOH溶液中滴入两滴酚酞的,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入O2,溶液颜色无明显变化。
①从实验Ⅲ和Ⅳ中,可得出的结论是___。
②同学们进一步通过实验证实了溶液a中滴入酚酞后,H2O2与酚酞发生了化学反应。实验方案是:取少量溶液a于试管中,___。