题目内容
14.下列各组物质在适宜条件下反应,其中氧化剂与还原剂的物质的量之比为2:1的是( )| A. | H2SO4(浓)+C | B. | Fe2O3+Al | C. | HNO3(浓)+C | D. | Fe2O3+CO |
分析 由发生的反应结合元素的化合价判断氧化剂、还原剂,利用反应确定氧化剂与还原剂物质的量之比为2:1,以此来解答.
解答 解:A.发生2H2SO4(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+2SO2↑+CO2↑,S元素的化合价降低,C元素的化合价升高,则H2SO4为氧化剂,C为还原剂,物质的量比为2:1,故A选;
B.发生Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,Al元素的化合价升高,Fe元素的化合价降低,则Fe2O3为氧化剂,Al为还原剂,物质的量比为4:1,故B不选;
C.发生4HNO3(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+CO2↑+4NO2↑,C元素的化合价升高,N元素的化合价降低,则HNO3为氧化剂,C为还原剂,物质的量比为1:2,故C不选;
D.发生Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe,C元素的化合价升高,Fe元素的化合价降低,则Fe2O3为氧化剂,CO为还原剂,物质的量比为1:3,故D不选;
故选A.
点评 本题考查氧化还原反应,把握发生的反应及反应中元素的化合价变化为解答的关键,注意从元素化合价角度分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.NA表示阿伏加德罗常数,下列说法错误的是( )
| A. | 5.6gFe与Br2完全反应,转移电子数为0.3NA | |
| B. | 常温常压下,3.2gO3所含的氧原子数为0.2NA | |
| C. | 1L 0.1mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和小于0.1NA | |
| D. | 常温常压下,22.4LO2所含的原子数为2NA |
5.下列说法错误的是( )
| A. | 金属钠着火可用干燥沙土扑灭 | |
| B. | 地沟油经处理后可用作生物柴油 | |
| C. | 糖类、油脂、蛋白质均为高分子化合物 | |
| D. | 氢氧化铁胶体的分散质粒子能通过滤纸孔隙 |
2.下列离子方程式书写正确的是( )
| A. | 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3•H2O+H2O | |
| B. | 氯化铝溶液中加入过量的氨水:Al3++4 NH3•H2O=4NH4++AlO2-+2H2O | |
| C. | 向次氯酸钙溶液中通入少量的二氧化硫:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO | |
| D. | 碳酸钠溶液中加入过量的苯酚: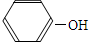 +CO32-= +CO32-= +HCO3- +HCO3- |
9.下列有关胶体和溶液的比较中,正确的是( )
| A. | 溶液中溶质粒子不带电,胶体分散质粒子带电 | |
| B. | 溶液中溶质的粒子运动有规律,胶体粒子运动无规律 | |
| C. | 通直流电后,溶液中溶质的粒子分别向两极运动,而胶体中分散质的粒子向某一极运动 | |
| D. | 溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现光亮的“通路” |
19.t℃时,CuSO4在水中的溶解度为25g,将32gCuSO4白色粉末加入mg水中形成饱和CuSO4溶液并有CuSO4•5H2O晶体析出,则m的取值范围是( )
| A. | 18g≤m≤128g | B. | 36g<m<180g | C. | 18g<m<128g | D. | 36g≤m≤180g |
6.根据下列反应判断有关物质还原性由强到弱的顺序是( )
H2SO3+I2+H2O═2HI+H2SO4 2FeCl3+2HI═2FeCl2+2HCl+I2
3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
H2SO3+I2+H2O═2HI+H2SO4 2FeCl3+2HI═2FeCl2+2HCl+I2
3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
| A. | NO>FeCl2>H2SO3>HI | B. | HI>FeCl2>H2SO3>NO | ||
| C. | FeCl2>HI>H2SO3>NO | D. | H2SO3>HI>FeCl2>NO |
3.下列溶液中与50mL 1mol•L-1的AlCl3溶液中氯离子浓度相等的是( )
| A. | 150mL1mol•L-1 的NaCl | B. | 75mL2 mol•L-1 的NH4Cl | ||
| C. | 150mL3mol•L-1的KCl | D. | 75mL2mol•L-1的CaCl2 |
4.下列叙述中,正确的是( )
| A. | 同物质的量的NaCl和Cl2含有的分子数相等 | |
| B. | SO42-的摩尔质量是96g | |
| C. | 阿伏伽德罗常数约为6.02×1023mol-1 | |
| D. | 1摩尔氧气的质量等于NA个O2分子的相对分子质量 |