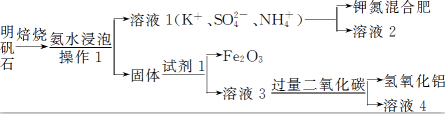
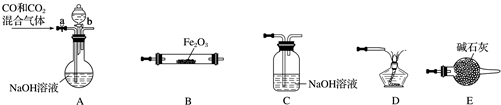
题目内容
5.下列说法错误的是( )| A. | 金属钠着火可用干燥沙土扑灭 | |
| B. | 地沟油经处理后可用作生物柴油 | |
| C. | 糖类、油脂、蛋白质均为高分子化合物 | |
| D. | 氢氧化铁胶体的分散质粒子能通过滤纸孔隙 |
分析 A.钠着火时生成过氧化钠,而过氧化钠能与水、二氧化碳发生反应生成氧气,不能使用水、干粉灭火器等来扑灭;
B.地沟油主要成分仍然是高级脂肪酸甘油酯,经加工处理后,可用来制肥皂和生物柴油;
C.葡萄糖、果糖属于糖类,但是不是高分子化合物;
D.胶体粒度小于滤纸空隙.
解答 解:A.钠着火时生成过氧化钠,而过氧化钠能与水、二氧化碳发生反应生成氧气,可用干燥沙土隔绝空气扑灭,故A正确;
B.地沟油主要成分仍然是高级脂肪酸甘油酯,经加工处理后,可用来制肥皂和生物柴油,有利于环境保护和资源再利用,故B正确;
C.糖类不全都是高分子化合物,例如葡萄糖、果糖,故C错误;
D.胶体粒度小于滤纸空隙,能够通过滤纸,故D正确;
故选:C.
点评 本题考查了物质的性质,熟悉钠、高级脂肪酸甘油酯、高分子化合物、胶体的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
15.下列各组离子在透明溶液中能大量共存的是( )
| A. | K+、Cu2+、Na+、Cl- | B. | H+、Na+、NO3-、CO32- | ||
| C. | Ba2+、H+、NO3-、SO42- | D. | Mg2+、Na+、OH-、SO42- |
13.下列说法正确的是( )
| A. | 加入铝粉能产生H2的溶液中,可能存在大量的Na+、Ba2+、AlO2-、NO3- | |
| B. | SO2通入碘水中,反应的离子方程式为SO2+I2+2H2O═SO32-+2I-+4H+ | |
| C. | 25℃时NH4Cl溶液的KW大于100℃时NaCl溶液的KW | |
| D. | 100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
10.25℃时,在pH=13的溶液中可以大量共存的离子组是( )
| A. | K+、Na+、HCO3-、NO3- | B. | Na+、K+、SO42-、Cl- | ||
| C. | H+、Mg2+、SO42-、NO3- | D. | Ag+、K+、NO3-、Na+ |
17.影响水的电离平衡的因素,观察下表的数据:
(1)从以上数据中发现什么递变规律?随着温度的升高,KW的值增大
(2)以上数据说明温度与水的电离程度之间存在什么关系?
[小结]:在H2O?H++OH-:
升高温度,水的电离程度增大,水的电离平衡向正向移动,KW增大.
降低温度,水的电离程度减小,水的电离平衡向逆向移动,KW减小.
| t(℃) | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
| Kw/10-14 | 0.134 | 0.292 | 0.681 | 1.01 | 2.92 | 5.47 | 38.0 | 55.0 |
(2)以上数据说明温度与水的电离程度之间存在什么关系?
[小结]:在H2O?H++OH-:
升高温度,水的电离程度增大,水的电离平衡向正向移动,KW增大.
降低温度,水的电离程度减小,水的电离平衡向逆向移动,KW减小.
14.下列各组物质在适宜条件下反应,其中氧化剂与还原剂的物质的量之比为2:1的是( )
| A. | H2SO4(浓)+C | B. | Fe2O3+Al | C. | HNO3(浓)+C | D. | Fe2O3+CO |
15.下列物质的保存方法正确的是( )
| A. | 少量金属钠保存在冷水中 | |
| B. | 浓硝酸盛放在无色瓶中 | |
| C. | 少量白磷保存在煤油中 | |
| D. | 氢氧化钠溶液盛放在橡胶塞的试剂瓶中 |