题目内容
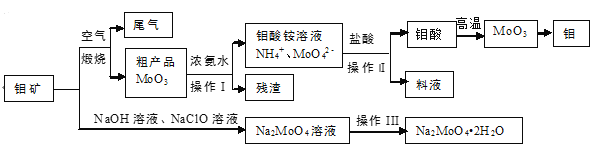
【题目】金属钼具有高强度、高熔点、耐磨抗腐性,用于制火箭、卫星的合金构件。钼酸钠晶体(Na2MoO42H2O)是一种重要的金属缓蚀剂。利用钼矿(主要成分MoS2,还含少量钙、镁等元素)为原料冶炼金属钼和钼酸钠晶体的主要流程图如下:
(1)Na2MoO42H2O中钼元素的价态为___,煅烧产生的尾气引起的环境危害主要是_______。
(2)用浓氨水溶解粗产品的离子方程式是_________,由图中信息可以判断MoO3是___氧化物。(填“酸性”、“碱性”或“两性”)
(3)操作I是_____,操作Ⅱ所得的钼酸要水洗,检验钼酸是否洗涤干净的方法是____。
(4)采用 NaClO氧化钼矿的方法将矿石中的钼浸出,该过程放热。
①请配平以下化学反应:
___NaClO +___MoS2 + ___NaOH →___Na2MoO4 +___Na2SO4 +___NaCl +___H2O。
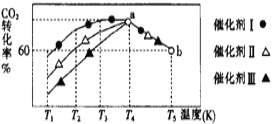
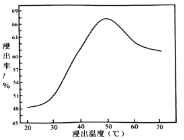
②钼的浸出率随着温度变化如图,当温度高于50℃后浸出率降低的可能原因是______(写一点)。
(5)锂和MoS2可充电电池的工作原理为xLi+nMoS2![]() Lix(MoS2)n,则电池充电时阳极上的电极反应式为______。
Lix(MoS2)n,则电池充电时阳极上的电极反应式为______。
【答案】+6 酸雨 MoO3 +2NH3H2O=2NH4+ + MoO42﹣+H2O 酸性 过滤 取少量最后一次水洗液于试管中,加入硝酸酸化的AgNO3溶液,若无沉淀产生即证明钼酸已洗净 9 1 6 1 2 9 3 该反应为放热反应,升温使平衡逆移;随着温度升高,其它金属杂质离子浸出也增多,沉淀了MoO42﹣ Lix(MoS2)n-xe﹣=nMoS2+xLi+
【解析】
制备金属钼和钼酸钠:钼矿的主要成分为MoS2,在空气中煅烧2MoS2+7O2![]() 2MoO3+4SO2,生成MoO3和SO2,所以尾气含SO2;MoO3加浓氨水生成钼酸铵溶液,2NH3H2O+MoO3=(NH4)2MoO4+H2O,过滤除去杂质,在钼酸铵溶液中加足量盐酸,发生复分解反应生成钼酸和氯化铵,过滤得到钼酸晶体高温分解生成MoO3;钼矿与NaOH、NaClO溶液发生反应9MoS2+6OH-+ClO-=MoO42-+2SO42-+9Cl-+3H2O,Na2MoO4溶液通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到Na2MoO4·2H2O。
2MoO3+4SO2,生成MoO3和SO2,所以尾气含SO2;MoO3加浓氨水生成钼酸铵溶液,2NH3H2O+MoO3=(NH4)2MoO4+H2O,过滤除去杂质,在钼酸铵溶液中加足量盐酸,发生复分解反应生成钼酸和氯化铵,过滤得到钼酸晶体高温分解生成MoO3;钼矿与NaOH、NaClO溶液发生反应9MoS2+6OH-+ClO-=MoO42-+2SO42-+9Cl-+3H2O,Na2MoO4溶液通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到Na2MoO4·2H2O。
(1) Na2MoO4·2H2O中Na元素化合价为+1价、O元素化合价为-2价,根据化合物中各元素化合价的代数和为0确定Mo元素的价态为4×2-2×1=+6价;工业煅烧钼矿的尾气为二氧化硫,二氧化硫引起的环境危害主要是酸雨;
(2)用浓氨水溶解粗产品MoO3,反应产生钼酸铵和水,反应的离子方程式为:MoO3 +2NH3H2O=2NH4+ + MoO42﹣+H2O;MoO3可以与碱溶液反应生成MoO42-和水,因此可以说明MoO3是酸性氧化物;
(3)操作I是分离难溶性的固体与可溶性液体混合物的方法,该分离混合物的方法为过滤;操作Ⅱ过滤分离出固体钼酸和滤液,在滤液中含有NH4Cl,所得的钼酸要水洗,检验钼酸是否洗涤干净的方法就是检验洗涤液中是否含有Cl-,操作是取少量最后一次水洗液于试管中,加入硝酸酸化的AgNO3溶液,若无沉淀产生即证明钼酸已洗净;
(4)①在该反应中Cl元素化合价由反应前NaClO 中的+1价变为反应后NaCl 中的-1价、Mo元素化合价由反应前MoS2中的+2价变为+6价、S元素化合价由反应前MoS2中的-1价变为反应后Na2SO4中的+6价,根据转移电子及原子守恒,配平方程式为9NaClO+MoS2+6NaOH=Na2MoO4+2Na2SO4+9NaCl+3H2O;
②钼的浸出率随着温度变化如图,当温度低于50℃时,温度升高,反应速率加快,更多的钼溶解,因此钼的浸出率随着温度的升高而增大;当温度高于50℃后浸出率降低的可能原因是:第一,该反应的正反应是放热反应,随着温度升高,平衡向吸热的逆反应方向移动;第二,随着温度升高,其它金属杂质离子浸出也增多,沉淀了MoO42﹣,导致浸出率降低;
(5)锂和MoS2可充电电池的工作原理为xLi+nMoS2![]() Lix(MoS2)n,可知:在电池充电时阳极上的电极反应式为放电时正极反应式的逆反应,放电时,正极上MoS2得电子和锂离子反应生成Lix(MoS2)n,则阳极反应式为Lix(MoS2)n-xe-=nMoS2+xLi+。
Lix(MoS2)n,可知:在电池充电时阳极上的电极反应式为放电时正极反应式的逆反应,放电时,正极上MoS2得电子和锂离子反应生成Lix(MoS2)n,则阳极反应式为Lix(MoS2)n-xe-=nMoS2+xLi+。

 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案【题目】FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下两种方法来制备无水FeCl2。有关物质的性质如下:
| C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 |
溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯, 易溶于乙醇,易吸水 | ||
熔点/℃ | -45 | 53 | 易升华 | |
沸点/℃ | 132 | 173 | ||
(1)用H2还原无水FeCl3制取FeCl2。有关装置如下:

①H2还原无水FeCl3制取FeCl2的化学方程式为_____________。
②按气流由左到右的方向,上述仪器的连接顺序为_________(填字母,装置可多次使用);C中盛放的试剂是_____________。
③该制备装置的缺点为________________。
(2)利用反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按下图装置,在三颈烧瓶中放入32.5g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。

①仪器a的名称是__________。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用的试剂可以是____,回收滤液中C6H5C1的操作方法是______。
③反应后将锥形瓶中溶液配成250mL,量取25.00mL所配溶液,用0.40mol/LNaOH溶液滴定,终点时消耗NaOH溶液为19.60 mL,则氯化铁的转化率为__________。
④为了减少实验误差,在制取无水FeCl2过程中应采取的措施有:________(写出一点即可)。