题目内容
2. 氯气的制取按照传统的方法,一般采用浓盐酸与MnO2共热来制备氯气,但是这种方法制过程中存在缺陷.某学习小组采用新的方法来制备氯气并进行性质实验.
氯气的制取按照传统的方法,一般采用浓盐酸与MnO2共热来制备氯气,但是这种方法制过程中存在缺陷.某学习小组采用新的方法来制备氯气并进行性质实验.(1)实验仪器及药品:
a.实验仪器:玻璃片、表面皿(顶部贴有湿润的蓝色石蕊试纸和干燥的石蕊试纸)、胶头滴管等
b.实验药品:KMnO4晶体、稀HCl、KBr溶液、淀粉溶液、KI溶液、FeSO4溶液、NaOH溶液、酚酞、KSCN溶液、AgNO3溶液、湿润的蓝色石蕊试纸和干燥的石蕊试纸.
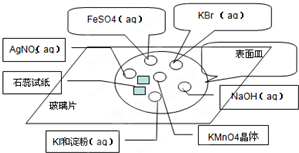
(2)实验方法及图示:
①在玻璃片上分别滴加KBr溶液、FeSO4溶液、NaOH稀溶液、KI溶液、AgNO3溶液.
②在KI溶液中滴加一滴淀粉溶液
③FeSO4溶液中滴加一滴KSCN溶液
④NaOH稀溶液中滴加一滴酚酞溶液
⑤在以上溶液分布的中心放置一块KMnO4晶体,然后滴加2-3滴稀盐酸,迅速盖上表面皿.并观察实验现象.
请回答下列问题:
(1)该反应实验原理:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
该反应中氧化剂与还原剂的物质的量之比为1:5;
(2)实验时反应一段时间后可以观察到KBr溶液由无色变为橙色,其离子反应方程式为Cl2+2Br-=2Cl-+Br2;
(3)滴有KSCN溶液的FeSO4溶液呈红色,其离子反应方程式为Cl2+2Fe2+=2Cl-+2Fe3+、Fe3++SCN-=Fe(SCN)3;
(4)滴加淀粉溶液的KI溶液呈蓝色,湿润的蓝色石蕊试纸的变化为先变红后褪色,干燥的石蕊试纸的变化为无变化.
分析 (1)分析反应中元素化合价变化,所含元素化合价升高的为还原剂,所含元素化合价降低为氧化剂;
(2)氯气氧化性强于溴,氯气与溴离子反应生成单质溴,溴水为橙色;
(3)氯气能够氧化二价铁离子生成三价铁离子,三价铁离子遇到KSCN溶液显血红色;
(4)氯气具有强的氧化性,能够氧化碘离子生成单质碘,碘遇到淀粉变蓝,氯气不具有漂白性,氯气与水反应生成盐酸与次氯酸,盐酸具有酸性,次氯酸具有漂白性.
解答 解:(1)2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O中,高锰酸钾中锰元素化合价降低,为氧化剂,氯化氢中氯元素化合价升高,为还原剂,参加反应的高锰酸钾中锰元素化合价都降低,所以氧化剂物质的量为2mol,参加反应的氯化氢16mol,只有10mol氯化氢中氯元素化合价升高,做还原剂,氧化剂与还原剂的物质的量之比为:1:5;
故答案为:1:5;
(2)氯气氧化性强于溴,氯气与溴离子反应生成单质溴,离子方程式:Cl2+2Br-=2Cl-+Br2,溴水为橙色;
故答案为:橙; Cl2+2Br-=2Cl-+Br2;
(3)氯气能够氧化二价铁离子生成三价铁离子,离子方程式:Cl2+2Fe2+=2Cl-+2Fe3+;三价铁离子遇到KSCN溶液显血红色,离子方程式:Fe3++SCN-=Fe(SCN)3;
故答案为:红; Cl2+2Fe2+=2Cl-+2Fe3+;Fe3++SCN-=Fe(SCN)3;
(4)氯气具有强的氧化性,能够氧化碘离子生成单质碘,碘遇到淀粉变蓝;氯气不具有漂白性,氯气与水反应生成盐酸与次氯酸,盐酸具有酸性,次氯酸具有漂白性,所以湿润的蓝色石蕊试纸的变化为:先变红后褪色;氯气不具有漂白性,干燥的石蕊试纸的变化无变化;
故答案为:蓝;先变红后褪色;无变化.
点评 本题考查了氯气的性质,明确氯气的性质是解题关键,注意氯水的成分及性质,注意氯气不具有漂白性,题目难度不大.

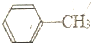 =2KMnO4$\stackrel{△}{→}$
=2KMnO4$\stackrel{△}{→}$ +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O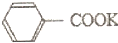 +HCl→
+HCl→ +KCl
+KCl实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.
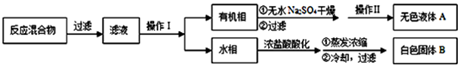
已知:苯甲酸相对分分子质量122,熔点122.4℃,在25℃和95℃时溶解度度分别为0,.3g和6.9g;纯净固体有机物一般都有固定熔点.
(1)操作I为分液,操作II为蒸馏.
(2)无色液体A是甲苯,定性区分苯和A的试剂常采用酸性高锰酸钾溶液,现象是紫色溶液褪色.
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔.该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表
明推测正确.请完成表中内容.
| 序号 | 实验方案 | 试验现象 | 结论 |
| ① | 将白色固体B加入水中,加热 溶解,冷却过滤 | 得到白色晶体和无色滤液 | |
| ② | 取少量滤液于试管中, 滴入适量的硝酸酸化的AgNO3溶液 | 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体,加热使其熔化, 测得熔点 | 测得熔点为122.4℃ | 白色晶体是苯甲酸 |
| A. | 用明矾净化饮用水 | |
| B. | 放电影时,放映室射到银幕上的光柱 | |
| C. | 氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 | |
| D. | 滚滚长江流入大海处,形成长江三角沙洲 |
| A. | 实验剩余的药品不能放回原试剂瓶 | |
| B. | 气体实验装置在实验前进行气密性检查 | |
| C. | 滴管不能交叉使用 | |
| D. | 如果少量酒精失火燃烧,可用湿抹布盖灭火焰 |
 某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体的装置(省略夹持装置,气密性已检查)如图所示.下列推断不合理的是( )
某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体的装置(省略夹持装置,气密性已检查)如图所示.下列推断不合理的是( )| A. | 烧杯中H2O2溶液作用是将Fe2+氧化为Fe3+ | |
| B. | a中的氧化铁与盐酸反应生成氯化铁 | |
| C. | b中收集到的气体是氢气 | |
| D. | 烧杯中溶液蒸发结晶得到氯化铁晶体 |
| A. | 电子流出的极 | B. | 电子流入的极 | ||
| C. | 发生氧化反应的极 | D. | 电极自身参与反应的极 |