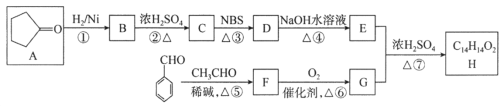
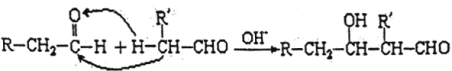
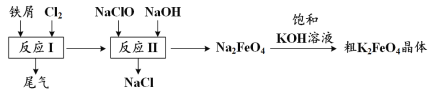��Ŀ����
����Ŀ���±���Ԫ�����ڱ���һ���֡��밴Ҫ����գ�
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
1 | ||||||||
2 | �� | �� | �� | �� | �� | |||
3 | �� | �� | �� | �� | �� |
(1)���Т�~���Ԫ���У�ԭ�Ӱ뾶������________(���������)���ǽ�������ǿ��Ԫ����________(���������)������������Ӧ��ˮ������������ǿ����_______(���������)����ѧ�������ȶ�����________(���������)��
(2)Ԫ�آ۵ij����⻯��ĵ�ʽΪ_________�����⻯����Ԫ�آ���⻯�ﻯ�Ϻ�����ˮ��ˮ��Һ������Ũ���ɴ�С��˳����________(�����ӷ��ű�ʾ)��
(3)��Ԫ�آߵĵ�����ɰֽ��ĥ���ϼ���![]() ��ҺƬ�̺������γɰ�ɫë״���ë״��Ļ�ѧʽ��______________����Ԫ�آߵĵ��ʵķ�ĩ���������ڸ����·�Ӧ��ų������ȣ�д���÷�Ӧ�Ļ�ѧ����ʽ____________
��ҺƬ�̺������γɰ�ɫë״���ë״��Ļ�ѧʽ��______________����Ԫ�آߵĵ��ʵķ�ĩ���������ڸ����·�Ӧ��ų������ȣ�д���÷�Ӧ�Ļ�ѧ����ʽ____________
���𰸡��� �� �� �� ![]() c(Cl-)>c(NH4+)>c(H+)>c(OH-) Al2O3 2Al+Fe2O3
c(Cl-)>c(NH4+)>c(H+)>c(OH-) Al2O3 2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
��������
��ͼ�е�λ�ù�ϵ��֪����Li������C������N������O������F������Na������Al������S������Cl������Ar��
��1��ͬһ����ԭ�Ӱ뾶��������С��ͬһ����ԭ�Ӱ뾶���ϵ�������������ϡ��������⣬ԭ�Ӱ뾶��������ԭ�ӣ�ͬһ���ڴ����ҷǽ���������ǿ��ͬһ������ϵ��·ǽ��������������Զ����ڷǽ�������ǿ���Ƿ�Ԫ�أ�����������������ˮ����������ǿԪ������Ԫ�أ����Т�~���Ԫ���У���ѧ�������ȶ�����̼Ԫ�أ�
�ʴ�Ϊ���ޣ� �� ���� ���ڣ�
��2��Ԫ�آ۵ij����⻯����NH3������ʽ��![]() ����������Ԫ�آ���⻯�ﻯ�Ϻ������Ȼ�泥�����ˮ������笠����Ӻ������ӣ�笠�����ˮ������һˮ�ϰ��������ӣ���Һ�����ԣ�����Ũ�ȵĴ�С��c(Cl-)>c(NH4+)>c(H+)>c(OH-)��
����������Ԫ�آ���⻯�ﻯ�Ϻ������Ȼ�泥�����ˮ������笠����Ӻ������ӣ�笠�����ˮ������һˮ�ϰ��������ӣ���Һ�����ԣ�����Ũ�ȵĴ�С��c(Cl-)>c(NH4+)>c(H+)>c(OH-)��
�ʴ�Ϊ�� ![]() ��c(Cl-)>c(NH4+)>c(H+)>c(OH-)��
��c(Cl-)>c(NH4+)>c(H+)>c(OH-)��
(3)Ԫ�آߵĵ��ʼ�������ɰֽ��ĥ��ȥ��������������������ϵμ����ṯ��Һ�����û���Ӧ���γ������룬��Ѹ�ٱ�����������������ë�������������췢�����ȷ�Ӧ����Ӧ�ķ���ʽ��2Al+Fe2O3![]() 2Fe+Al2O3��
2Fe+Al2O3��
�ʴ�Ϊ��Al2O3��2Al+Fe2O3![]() 2Fe+Al2O3��
2Fe+Al2O3��

����Ŀ��FeSO4��Һ�����ڿ��������ױ��ʣ����Ϊ�˷���ʹ��Fe2+��ʵ�����г�������������茶���[�׳ơ�Ħ���Ρ�����ѧʽΪ(NH4)2Fe(SO4)26H2O]�������̷����̷���Һ���ȶ���
I��ij��ȤС�����ʵ���Ʊ���������茶��塣
��ʵ���У�������Һ�Լ�����ʹ�õ�������ˮ��������С���ȴ����ʹ�á���FeSO4��Һ�м��뱥��(NH4)2SO4��Һ����������_______����ȴ�ᾧ�����ˡ�ϴ�Ӻ����õ�һ��dz����ɫ�ľ��塣
II��ʵ��̽��Ӱ����Һ��Fe2+�ȶ��Ե�����
(1)����0.8 mol/L��FeSO4��Һ��pH=4.5����0.8 mol/L��(NH4)2Fe(SO4)2��Һ��pH=4.0������ȡ2 mL������Һ����֧�Թ��У��տ�ʼ������Һ����dz��ɫ���ֱ�ͬʱ�μ�2��0.01mol/L��KSCN��Һ��15min��۲�ɼ���(NH4)2Fe(SO4)2��Һ��ȻΪdz��ɫ��������Һ��FeSO4��Һ����ֵ���ɫ���ǡ�
������1��
���� | Fe(OH)2 | Fe(OH)3 |
��ʼ���� pH | 7.6 | 2.7 |
��ȫ���� pH | 9.6 | 3.7 |
���������ӷ���ʽ����FeSO4��Һ��������ɫ���ǵ�ԭ��___________________��
������Ӱ��Fe2+�ȶ��Ե����أ�С��ͬѧ�������3�ּ��裺
����1������������ͬʱ��NH4+�Ĵ���ʹ(NH4)2Fe(SO4)2��Һ��Fe2+�ȶ��ԽϺá�
����2������������ͬʱ����һ�� pH��Χ�ڣ���Һ pHԽСFe2+�ȶ���Խ�á�
����3��__________________________________________________��
(2)С��ͬѧ����ͼװ�ã�GΪ���������ƣ�������������������Һ�ֱ������ҺA��0.2 mol/L NaCl������ҺB��0.1mol/L FeSO4��Ϊ��ͬ�� pH���۲��¼�����ƶ������Լ���2����ʵ���о���ʵ�������±���ʾ��
��� | A 0.2mol/LNaCl | B 0.1mol/LFeSO4 | �����ƶ��� |
ʵ��1 | pH=1 | pH=5 | 8.4 |
ʵ��2 | pH=1 | pH=1 | 6.5 |
ʵ��3 | pH=6 | pH=5 | 7.8 |
ʵ��4 | pH=6 | pH=1 | 5.5 |
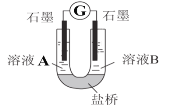
������2��ԭ���װ���У�����������ͬʱ��������Ӧ��Ļ�ԭ��Խǿ��������Ӧ���������Խǿ����ԭ��صĵ���Խ��
������3�������£�0.1mol/LpH=1��FeSO4��Һ��pH=5��FeSO4��Һ�ȶ��Ը��á�
��������ʵ������������Ϣ����С�����ۿ��Եó����½��ۣ�
��U������صĵ缫��Ӧʽ_________________��
�ڶԱ�ʵ��1��2����3��4������һ��pH��Χ�ڣ��ɵó��Ľ���Ϊ______ ��
�۶Ա�ʵ��_____��_____ ���ɵó���һ�� pH��Χ�ڣ���Һ����Ա仯�Ƕ�O2������ǿ����Ӱ�����ء�
�ܶԣ�����3��ʵ����ʵ�Ľ���Ϊ____________________��