题目内容
【题目】A~G都是有机化合物,它们的转化关系如下:

请回答下列问题:
(1)已知:6.0 g化合物E完全燃烧生成8.8 g CO2和3.6 g H2O;E的蒸气对氢气的相对密度为30,则E的分子式为_______________。
(2)A为一取代芳烃,B中含有一个甲基。由B生成C的化学方程式为 。
(3)由B生成D、由C生成D的反应条件分别是_______________、_______________。
(4)由A生成B、由D生成G的反应类型分别是_______________、_______________。
(5)F存在于栀子香油中,其结构简式为_______________。
![]() 【答案】(1) C2H4O2 (2)
【答案】(1) C2H4O2 (2)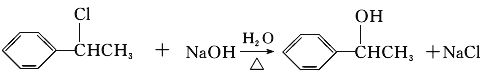
(3)NaOH的醇溶液,加热;浓硫酸,加热
(4)取代反应,加成反应 (5)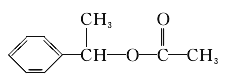
【解析】
试题分析:(1)E蒸气的密度标准状况下约为2.68g/L,则E的摩尔质量=22.4×2.68=60g/mol,6.0gE的物质的量是0.1mol,完全燃烧后生成8.8 g CO2和3.6g H2O,物质的量分别为0.2mol、0.2mol,则分子中N(C)=2、N(H)=4,故N(O)=(60-24-4)/16=2,所以E的分子式是C2H4O2;
(2)A为一取代芳香烃,由分子式C8H10可知为苯的同系物,故A为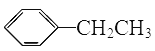 ,A与氯气在光照条件下发生取代反应生成B,而B中含有一个甲基,则B为
,A与氯气在光照条件下发生取代反应生成B,而B中含有一个甲基,则B为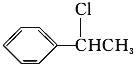 ,B发生水解反应生成C为
,B发生水解反应生成C为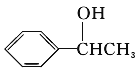 ,由B生成C的化学方程式为
,由B生成C的化学方程式为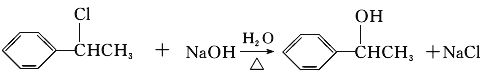 ;
;
(3)C与E发生反应生成F,结合F的分子式可知,应是发生酯化反应,则E为CH3COOH,F为 ,B、C转化都得到D,D与溴发生加成反应生成G,则B、C均发生消去反应生成D,故D为
,B、C转化都得到D,D与溴发生加成反应生成G,则B、C均发生消去反应生成D,故D为![]() ,则G为
,则G为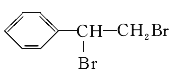 ,所以由B生成D的反应条件是NaOH醇溶液、加热;由C生成D的反应条件是浓硫酸、加热;
,所以由B生成D的反应条件是NaOH醇溶液、加热;由C生成D的反应条件是浓硫酸、加热;
(4)根据以上分析可知由A生成B是取代反应,由D生成G是加成反应;
(5)由上述分析可知F的结构简式为 。
。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
T | 最外层电子数是电子层数的3倍 |
Z | 元素最高正价是+7价 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是__________;X的一种氢化物燃烧时火焰温度高,可以焊接金属,则该氢化物的结构式为 ;实验室制取该气体的化学方程式是 。
(2)将9g单质X在足量氧气中燃烧,所得气体通入1L 1mol·L-1NaOH溶液中,完全吸收后,将溶液在减压低温条件下蒸干,得到不含结晶水的固体质量为 g。
(3)元素Y与氢元素形成一种离子YH,写出该微粒的电子式____________(用元素符号表示)。实验室检验该微粒的方法是: 。
(4)T元素在周期表的位置: ,其简单阴离子的结构示意图: , 证明该粒子的还原性比Z— 强的离子方程式是 。硒(Se)是人体必需的微量元素,与T在同一主族,Se原子比T原子多一个电子层,则Se的原子序数为________,其最高价氧化物对应的水化物的化学式为________。
(5)元素Z与氢氧化钠溶液反应的化学方程式为 ,其生成的含氧酸盐的电子式为 。