��Ŀ����
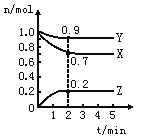
����Ŀ��ij�¶�ʱ����һ��2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ�����д���пհף�
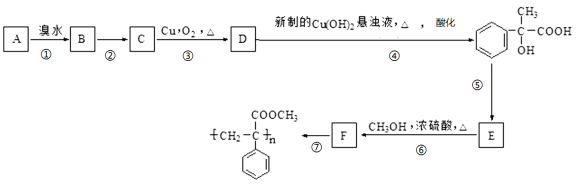
��1���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��2����Ӧ��ʼ��2min��������Z��ʾ��ƽ����Ӧ����Ϊ ��
��3����X��Y��Z��Ϊ���壬2min��Ӧ�ﵽƽ�⣬��Ӧ��ƽ��ʱ������ʱ��ϵ��ѹǿ�ǿ�ʼʱ�� ����
����ƽ��ʱ�������ڻ�������ƽ������������ʼͶ��ʱ_______ _____(��������������С�����������)��
���𰸡���1��3X+Y ![]() 2Z��
2Z��
��2��0.05mol/(L��min)��
��3��0.9 �� ����
��������
�����������1������ͼ����Կ�����X��Y�����ʵ�����С��Z�����ʵ�����������X��YΪ��Ӧ�ZΪ�����2min��X��Y�����ʵ���Ϊ��ֵ�Ҳ�Ϊ�㣬Ϊ���淴Ӧ����ͬʱ�������ʵ����ı仯��ֵΪ����n(X):��n(Y):��n(Z)=(1.0-0.7)mol:(1.0-0.9)mol:0.2mol=3:1:2����ѧ����ʽΪ3X+Y ![]() 2Z���ʴ�Ϊ��3X+Y
2Z���ʴ�Ϊ��3X+Y ![]() 2Z��
2Z��
��2������Ӧ��ʼ��2min������Z��ƽ����Ӧ����Ϊv=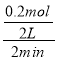 =0.05mol/(L��min)���ʴ�Ϊ��0.05mol/(L��min)��
=0.05mol/(L��min)���ʴ�Ϊ��0.05mol/(L��min)��
��3��������Ӧ��ƽ��ʱ������������ʵ���Ϊ��0.9mol+0.7mol+0.2mol=1.8mol����ʼʱ����������ʵ���Ϊ��1.0mol+1.0mol=2.0mol����Ӧ��ƽ��ʱ����ʱ�����ڵ�ѹǿ����ʼѹǿ֮��Ϊ1.8mol:2.0mol=9:10����ʱ��ϵ��ѹǿ�ǿ�ʼʱ�� 0.9�����ʴ�Ϊ��0.9��
��ƽ��ʱ����������ƽ��Ħ������=![]() ����������������䣬�����ʵ������٣���������ƽ��Ħ���������ʴ�Ϊ������
����������������䣬�����ʵ������٣���������ƽ��Ħ���������ʴ�Ϊ������

 ��ְٷְټ���ϵ�д�
��ְٷְټ���ϵ�д�����Ŀ��A��B��C����ǿ����ʣ�������ˮ�е�������������±���ʾ��
������ | Na����K����Cu2�� |
������ | SO��OH�� |
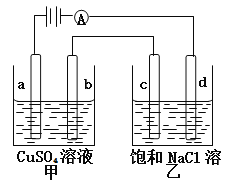
����ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��������A��Һ��������B��Һ��������C��Һ���缫��Ϊʯī�缫��

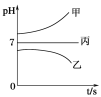
��ͨ��Դ������һ��ʱ�������ձ���c�缫����������16 g�������¸��ձ�����Һ��pH����ʱ��t�Ĺ�ϵ����ͼ���ݴ˻ش��������⣺
��1��MΪ��Դ��_____��(���������)���缫b�Ϸ����ĵ缫��ӦΪ__________________��
��2���缫e�����ɵ������ڱ�״̬�µ����Ϊ________��
��3��д�����ձ��еĵ��ط�Ӧ_______________________��
��4��Ҫʹ���ձ��е�C��Һ�ָ���ԭ����״̬����ȷ�IJ���__________�������������ݣ���