题目内容
【题目】Ⅰ:下列各项分别与哪个影响化学反应速率因素的关系最为密切?
(1)夏天的食品易变霉,在冬天不易发生该现象 ;
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢 ;
(3)MnO2加入双氧水中放出气泡更快 .
Ⅱ:在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:

(1)比较t2时刻,正逆反应速率大小V正 V逆.(填“>”、“=”、“<”)
(2)若t2=2min,计算反应开始至t2时刻用M的浓度变化表示的平均反应速率为: .
(3)t3时刻化学反应达到平衡,反应物的转化率为 .
(4)如果升高温度,则V逆 (填增大、减小或不变).
【答案】(1)温度;
(2)反应物本身性质;
(3)催化剂;
Ⅱ:(1)>;
(2)0.25mol/(Lmin);
(3)75%;
(4)增大;
【解析】
试题分析::Ⅰ:(1)夏天温度较高,反应速率较大,而冬天温度较低,反应速率较低,故答案为:温度;
(2)反应物本身性质是影响化学反应速率的主要因素,镁比锌活泼,与盐酸反应较剧烈,故答案为:反应物本身性质;
(3)二氧化锰为反应的催化剂,可加快反应速率,故答案为:催化剂;Ⅱ:(1)t2时刻,反应物逐渐减小,生成物逐渐增多,则反应向正向移动,V正>V逆,故答案为:>;(2)v=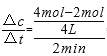 ==0.25mol/(Lmin),故答案为:0.25mol/(Lmin);(3)t3时刻化学反应达到平衡,剩余2molN,则转化6molN,转化率为(8-2)/8==75%,故答案为:75%;(4)升高温度,反应速率增多,故答案为:增大。
==0.25mol/(Lmin),故答案为:0.25mol/(Lmin);(3)t3时刻化学反应达到平衡,剩余2molN,则转化6molN,转化率为(8-2)/8==75%,故答案为:75%;(4)升高温度,反应速率增多,故答案为:增大。

 优学名师名题系列答案
优学名师名题系列答案【题目】A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Na+、K+、Cu2+ |
阴离子 | SO、OH- |
在下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。
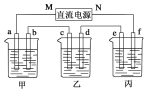
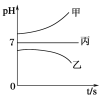
接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了16 g。常温下各烧杯中溶液的pH与电解时间t的关系如上图。据此回答下列问题:
(1)M为电源的_____极(填“正”或“负”),电极b上发生的电极反应为__________________。
(2)电极e上生成的气体在标准状态下的体积为________。
(3)写出乙烧杯中的电解池反应_______________________。
(4)要使丙烧杯中的C溶液恢复到原来的状态,正确的操作__________(计算出相关数据)。