题目内容
19.下列有关说法不正确的是( )| A. | 氯气通入淀粉碘化钾溶液中,溶液变蓝,氧化性:Cl2>I2 | |
| B. | 久置的氯水最终变为稀盐酸 | |
| C. | NaClO溶液的漂白原理与Na202相同,与SO2不同 | |
| D. | 无色溶液C中加入AgN03溶液,产生白色沉淀,再加入稀盐酸,沉淀不消失,则无色溶液C中一定含有Cl- |
分析 A.氯气通入淀粉碘化钾溶液中,溶液变蓝,说明氯气置换出碘;
B、氯水中存在次氯酸,次氯酸见光易分解;
C、根据NaClO、Na2O2的漂白原理为氧化漂白,SO2的漂白原理为化合漂白;
D、能和银离子反应生成白色沉淀的阴离子有碳酸根离子、氯离子等.
解答 解:A.氯气通入淀粉碘化钾溶液中,溶液变蓝,说明氯气置换出碘,发生Cl2+2I-=2Cl-+I2,可说明氧化性:Cl2>I2,故A正确;
B、氯气和水反应生成盐酸和次氯酸,次氯酸不稳定,见光易分解作为盐酸,故B正确;
C、因NaClO、Na2O2的漂白原理为氧化漂白,漂白原理相同,但是SO2的漂白原理为化合漂白,漂白原理和前二者不一样,故C正确;
D、在某溶液中加入AgNO3溶液有白色沉淀产生,该白色沉淀可能是碳酸银,碳酸银和盐酸反应转化为氯化银白色沉淀,所以原溶液中不一定含有氯离子,故D错误.
故选D.
点评 本题考查学生物质的性质以及常见阴离子的检验方法,难度不大,做题时注意从题目中找出反应的典型现象,根据物质的性质进行判断.

练习册系列答案
相关题目
10.在同一容器内有X、Y、Z、Q四种物质,在合适的条件下反应,反应前后各物质的质量如表,该反应属( )
| X | Y | Z | Q | |
| 反应前g | 20 | 20 | 20 | 20 |
| 反应后g | 10 | 20 | 26 | 24 |
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
7.下列叙述正确的是( )
| A. | 同温同压下,相同体积的气体,它们的物质的量必相等 | |
| B. | 任何条件下,等体积的O2和H2O所含的分子数必相等 | |
| C. | 1LCO气体一定比1LO2的质量小 | |
| D. | 等质量的N2和CO2两种气体的分子数一定相等 |
14.下列说法正确的是( )
| A. | 22.4LN2中一定含有6.02×1023个氮分子 | |
| B. | 1LH2O中溶解了0.5molNaCl,则该溶液的物质的量浓度为0.5mol/L | |
| C. | 从1L1mol/LC12H22O11溶液中取出10mL,则取出的10mL溶液物质的量的浓度仍为1mol/L | |
| D. | 1LH2SO4溶液中含有98g H2SO4,则该溶液的物质的量浓度为98g/L |
1.已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价Cr的强氧化性,其毒性是+3价Cr毒性的100倍.因此,必须对含铬的废水进行处理.目前研究和采用的处理方法主要有:
方法一、还原法:在酸性介质中用FeSO4、NaHSO3等将+6价Cr还原成+3价Cr.具体流程如下:

有关离子完全沉淀的pH如下表.
请回答下列问题:
(1)在②中调节pH的范围至B为最好.(填序号)
A.3~4 B.6~8 C.10~11 D.12~14
(2)若在①使FeSO4适当过量、空气适量,使Fe2+与Fe3+的比例恰当时,可产生具有磁性、组成类似于Fe3O4•xH2O的铁氧体悬浮物,变废为宝.则控制空气适量的目的是使溶液中Fe2+与Fe3+的比例恰当,使铁氧体分离出来较简便的方法是用磁铁吸引.
方法二、电解法:将含+6价Cr的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3十在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(3)写出此阴极反应的电极方程式2H2O+2e-═H2↑+2OH-.现用上法处理1×104 L含铬(+6价)78mg/L的废水,电解时阳极物质消耗的质量至少为2.52kg.
方法一、还原法:在酸性介质中用FeSO4、NaHSO3等将+6价Cr还原成+3价Cr.具体流程如下:

有关离子完全沉淀的pH如下表.
| Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | |
| Ksp | 8.0×10-16 | 4.0×10-38 | 6.0×10-31 |
| 完全沉淀的pH | 9.0 | 3.2 | 5.6 |
(1)在②中调节pH的范围至B为最好.(填序号)
A.3~4 B.6~8 C.10~11 D.12~14
(2)若在①使FeSO4适当过量、空气适量,使Fe2+与Fe3+的比例恰当时,可产生具有磁性、组成类似于Fe3O4•xH2O的铁氧体悬浮物,变废为宝.则控制空气适量的目的是使溶液中Fe2+与Fe3+的比例恰当,使铁氧体分离出来较简便的方法是用磁铁吸引.
方法二、电解法:将含+6价Cr的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3十在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(3)写出此阴极反应的电极方程式2H2O+2e-═H2↑+2OH-.现用上法处理1×104 L含铬(+6价)78mg/L的废水,电解时阳极物质消耗的质量至少为2.52kg.
2.X、Y、Z、W、Q均为短周期元素,其中Y、Z、W、Q在元素周期表中的相对位置,X是周期表中原子半径最小的元素,Q的原子序数是W的2倍.
(1)Z原子的结构示意图为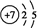 ,化合物X2Q的电子式为
,化合物X2Q的电子式为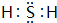 .
.
(2)可溶性盐(ZX4)2Q2W8是强氧化剂,可将二价锰离子氧化为高锰酸根离子,所得溶液呈强酸性,写出该反应的离子方程式:2Mn2++5S2O82-+8H2O=2MnO4-+10SO42-+16H+.
(3)一定条件下,向容积不变的密闭容器中充入a mol QW2与b mol YW,发生反应生成YW2和液态Q单质,反应达到平衡时转移2.5mol电子,同时放出85kJ热量,则该反应的热化学方程式为SO2(g)+2CO(g) 2CO2(g)+S(l)△H=-136 kJ•mol-1,欲使YW的平衡转化率大于QW2的平衡转化率,则a与b的关系为a:b>1:2.
2CO2(g)+S(l)△H=-136 kJ•mol-1,欲使YW的平衡转化率大于QW2的平衡转化率,则a与b的关系为a:b>1:2.
| Y | Z | W |
| Q |
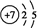 ,化合物X2Q的电子式为
,化合物X2Q的电子式为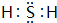 .
.(2)可溶性盐(ZX4)2Q2W8是强氧化剂,可将二价锰离子氧化为高锰酸根离子,所得溶液呈强酸性,写出该反应的离子方程式:2Mn2++5S2O82-+8H2O=2MnO4-+10SO42-+16H+.
(3)一定条件下,向容积不变的密闭容器中充入a mol QW2与b mol YW,发生反应生成YW2和液态Q单质,反应达到平衡时转移2.5mol电子,同时放出85kJ热量,则该反应的热化学方程式为SO2(g)+2CO(g)
 2CO2(g)+S(l)△H=-136 kJ•mol-1,欲使YW的平衡转化率大于QW2的平衡转化率,则a与b的关系为a:b>1:2.
2CO2(g)+S(l)△H=-136 kJ•mol-1,欲使YW的平衡转化率大于QW2的平衡转化率,则a与b的关系为a:b>1:2.