题目内容
7.下列叙述正确的是( )| A. | 同温同压下,相同体积的气体,它们的物质的量必相等 | |
| B. | 任何条件下,等体积的O2和H2O所含的分子数必相等 | |
| C. | 1LCO气体一定比1LO2的质量小 | |
| D. | 等质量的N2和CO2两种气体的分子数一定相等 |
分析 A.同温同压下,气体的体积之比等于其物质的量之比;
B.等体积的O2和H2O的物质的量不一定相等;
C.体积相同条件下,温度、压强会影响气体的物质的量;
D.根据n=$\frac{m}{M}$计算判断二者物质的量关系,若物质的量相等,则含有分子数目相等.
解答 解:A.同温同压下,由于气体摩尔体积相同,由V=nVm可知,相同体积的气体,它们的物质的量必相等,故A正确;
B.等体积的O2和H2O的物质的量不一定相等,则二者含有分子数目不一定相等,故B错误;
C.体积相同条件下,温度、压强会影响气体的物质的量,不能确定CO、氧气物质的量大小,不能确定二者质量大小关系,故C错误;
D.根据n=$\frac{m}{M}$可知,等质量的N2和CO2的物质的量之比为44g/mol:28g/mol=11:7,则二者含有分子数目之比为11:7,故含有分子数目不相等,故D错误,
故选:A.
点评 本题考查阿伏伽德罗定律及其推论,难度不大,注意根据PV=nRT理解阿伏伽德罗定律及其推论.

练习册系列答案
相关题目
18.A、B、C为短周期的三种元素,已知A、B处于同周期;A、C的最低价离子分别为A2-和C-;A2-的离子半径大于C-;B2+与C-具相同的电子层结构,以下叙述不正确的是( )
| A. | 原子半径B>A>C | B. | 原子序数A>B>C | ||
| C. | 离子半径A2->B2+>C- | D. | 最外层电子数C>A>B |
15.如图是初中化学常见的实验操作,其中错误的是( )
| A. |  给液体加热 | B. |  除去CO中的CO2 | C. | 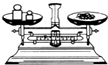 称量 | D. | 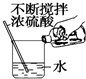 稀释浓硫酸 |
19.下列有关说法不正确的是( )
| A. | 氯气通入淀粉碘化钾溶液中,溶液变蓝,氧化性:Cl2>I2 | |
| B. | 久置的氯水最终变为稀盐酸 | |
| C. | NaClO溶液的漂白原理与Na202相同,与SO2不同 | |
| D. | 无色溶液C中加入AgN03溶液,产生白色沉淀,再加入稀盐酸,沉淀不消失,则无色溶液C中一定含有Cl- |
16.已知HNO2 在低温下比较稳定,酸性比醋酸略强,既有氧化性又有还原性,其氧化产物,还原产物与溶液PH的关系如表:
下列有关说法错误的是( )
| pH范围 | >7 | <7 |
| 产物 | NO3- | NO、N2O、N2中的一种 |
| A. | 碱性条件下,NaNO2与NaClO反应的离子方程式为NO2-+ClO-═NO3-+Cl- | |
| B. | 向冷的NaNO2溶液中通入CO2可得到HNO2 | |
| C. | 向冷的NaNO2溶液中加入稀硫酸可得到HNO2 | |
| D. | 向冷的NaNO2溶液中加入滴有淀粉的氢碘酸,溶液变蓝色 |
10.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 醋酸和水 | B. | 碘和苯 | C. | 水和溴苯 | D. | 汽油和煤油 |