题目内容
14.下列说法正确的是( )| A. | 22.4LN2中一定含有6.02×1023个氮分子 | |
| B. | 1LH2O中溶解了0.5molNaCl,则该溶液的物质的量浓度为0.5mol/L | |
| C. | 从1L1mol/LC12H22O11溶液中取出10mL,则取出的10mL溶液物质的量的浓度仍为1mol/L | |
| D. | 1LH2SO4溶液中含有98g H2SO4,则该溶液的物质的量浓度为98g/L |
分析 A.氮气所处状态的气体摩尔体积不一定是22.4L/mol;
B.1LH2O中溶解了0.5molNaCl,溶液的体积不是1L;
C.溶液是均一的,取出溶液浓度与原溶液浓度相等;
D.物质的量浓度为单位体积的溶液中含有溶质的物质的量.
解答 解:A.氮气所处状态的气体摩尔体积不一定是22.4L/mol,即22.4L氮气的物质的量不一定为1mol,含有的氮气分子数目不一定为6.02×1023个,故A错误;
B.1LH2O中溶解了0.5molNaCl,溶液的体积不是1L,其浓度不是0.5mol/L,故B错误;
C.溶液是均一的,取出溶液浓度与原溶液浓度相等,取出的10mL溶液物质的量的浓度仍为1mol/L,故C正确;
D.1LH2SO4溶液中含有98g H2SO4,硫酸物质的量为1mol,则该溶液的物质的量浓度为1mol/L,故D错误,
故选:C.
点评 本题考查气体摩尔体积、物质的量浓度、溶液性质等,比较基础,注意气体摩尔体积的使用条件与对象.

练习册系列答案
 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
4.在一个固定体积的密闭容器中,加入2molA和1molB,发生反应:2A(g)+B(g)?3C(g)+D(g),达到平衡时C的浓度为Wmol/L,若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为Wmol/L的是( )
| A. | 4molA+2molB | B. | 3molC+1molD+1molB | ||
| C. | 3molC+1molD | D. | 1.5molC+0.5molD |
5.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,等体积的水和CO2,含有的氧原子数目为1:2 | |
| B. | 含有NA个阴离子的Na2O2与足量水反应,转移电子数为2NA | |
| C. | 向含有1molFeI2的溶液中通入适量氯气,当有NA个Fe2+被氧化时,共转移电子数为3NA | |
| D. | 一个NO分子质量为a g,一个NO2分子质量是b g,则NA个O2的质量为(b-a)NAg |
19.下列有关说法不正确的是( )
| A. | 氯气通入淀粉碘化钾溶液中,溶液变蓝,氧化性:Cl2>I2 | |
| B. | 久置的氯水最终变为稀盐酸 | |
| C. | NaClO溶液的漂白原理与Na202相同,与SO2不同 | |
| D. | 无色溶液C中加入AgN03溶液,产生白色沉淀,再加入稀盐酸,沉淀不消失,则无色溶液C中一定含有Cl- |
3.已知不同金属离子在溶液中完全沉淀时,溶液的pH不同.
据信息分析除去CuCl2中的FeCl3应选用什么试剂,原理是什么?
| 溶液中被沉淀的离子 | Fe3+ | Cu2+ |
| 完全生成氢氧化物沉淀时溶液的pH | ≥3.7 | ≥4.4 |
17.某同学做元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验目的:研究同周期元素性质的递变规律.
(2)实验用品:
试剂:金属钠,镁条、铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞试液等.
仪器:①小刀,②胶头滴管,③酒精灯,试管,试管夹,烧杯,镊子,玻璃片,砂纸,滤纸,火柴等.
(3)实验内容:实验②对应的现象:(填相应字母);实验⑥对应的离子反应是Al3++4OH-=AlO2-+2H2O
(4)实验所有实验步骤最终得出的结论是:金属性:Na>Mg>Al 非金属性:Cl>S.
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞试液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色 |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③用小刀切割一小块钠擦干煤油后放入滴有酚酞试液的装有冷水的烧杯中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将打磨后的镁投入装有稀盐酸的试管中 | D.反应不十分剧烈,产生无色气体 |
| ⑤将打磨后的铝投入装有稀盐酸的试管中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向AlCl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀 |
(1)实验目的:研究同周期元素性质的递变规律.
(2)实验用品:
试剂:金属钠,镁条、铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞试液等.
仪器:①小刀,②胶头滴管,③酒精灯,试管,试管夹,烧杯,镊子,玻璃片,砂纸,滤纸,火柴等.
(3)实验内容:实验②对应的现象:(填相应字母);实验⑥对应的离子反应是Al3++4OH-=AlO2-+2H2O
(4)实验所有实验步骤最终得出的结论是:金属性:Na>Mg>Al 非金属性:Cl>S.

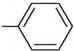 中的两种基团组成的化合物,与NaOH溶液恰好完全发生反应,反应后所得产物中再通入二氧化碳,也能发生反应的物质可能是苯酚钠、碳酸钠.
中的两种基团组成的化合物,与NaOH溶液恰好完全发生反应,反应后所得产物中再通入二氧化碳,也能发生反应的物质可能是苯酚钠、碳酸钠.