题目内容
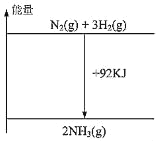
【题目】工业上可用一氧化碳合成可再生能源甲醇。
(1)已知:Ⅰ.3CO(g)+6H2(g)![]() CH3CH=CH2(g)+3H2O(g) △H1=-301.3kJ/mol;
CH3CH=CH2(g)+3H2O(g) △H1=-301.3kJ/mol;
Ⅱ.3CH3OH(g)![]() CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol。
CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol。
则CO与H2合成气态甲醇的热化学方程式为___________________________________
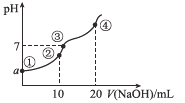
(2)某科研小组在Cu2O/ZnO作催化剂的条件下,在500℃时,研究了n(H2):n(CO)分别为2:1、5:2时CO的转化率变化情况(如图1所示),则图中表示n(H2):n(CO)=2:1的变化曲线为___________(填“曲线a”或“曲线b”),原因是_______________________________。
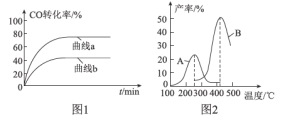
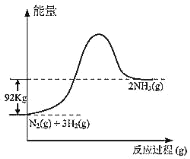
(3)某科研小组向密闭容器中充入一定量的CO和H2合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得CH3OH的产率与温度的关系如图2所示。下列说法正确的是____________(填选项字母)。
a.使用催化剂A能加快相关化学反应速率,但催化剂A并未参与反应
b.在恒温恒压的平衡体系中充入氩气,CH3OH的产率降低
c.当2v(CO)正=v(H2)逆时,反应达到平衡状态
(4)一定温度下,在容积均为2L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。

若甲容器平衡后气体的压强为开始时的![]() ,则该温度下,该反应的平衡常数K=______,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为_____________________________________。
,则该温度下,该反应的平衡常数K=______,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为_____________________________________。
(5)CO与日常生产生活相关。
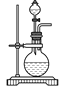
①检测汽车尾气中CO含量,可用CO分析仪,工作原理类似于燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2-。则负极的电极反应式为__________________。
②碳酸二甲醋[(CH3O)2CO]毒性小,是一种绿色化工产品,用CO合成(CH3O)2CO,其电化学合成原理为4CH3OH+2CO+O2![]() 2(CH3O)2CO+2H2O,装置如图3所示:
2(CH3O)2CO+2H2O,装置如图3所示:
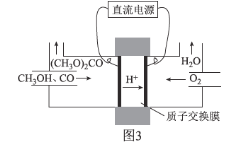
写出阳极的电极反应式:________________________________________
【答案】CO(g)+2H2(g)![]() CH3OH(g) △H=-90.1kJ/mol 曲线b H2的含量越低,CO的转化率越低 bc 0.25 1<c<2 CO+O2--2e-=CO2 2CH3OH+CO-2e-= (CH3O)2CO+2H+
CH3OH(g) △H=-90.1kJ/mol 曲线b H2的含量越低,CO的转化率越低 bc 0.25 1<c<2 CO+O2--2e-=CO2 2CH3OH+CO-2e-= (CH3O)2CO+2H+
【解析】
(1)根据盖斯定律解题;
(2)增加反应物浓度,平衡正向移动,增加的反应物转化率下降,其他反应物的转化率上升;
(3)催化剂可以同等程度加快反应速率,参加中间反应;根据平衡移动分析;
(4)利用三行式法计算k;根据等效平衡分析;
(5)根据负极氧化失电子,阳极氧化失电子分析。
(1)根据盖斯定律,(Ⅰ-Ⅱ)/3可得,CO(g)+2H2(g)![]() CH3OH(g) △H=-90.1kJ/mol;
CH3OH(g) △H=-90.1kJ/mol;
答案:CO(g)+2H2(g)![]() CH3OH(g) △H=-90.1kJ/mol
CH3OH(g) △H=-90.1kJ/mol
(2) 因为增加反应物浓度,平衡正向移动,增加的反应物转化率下降,其他反应物的转化率上升,则n(H2)/n(CO)越小,CO的转化率越小,故曲线b表示n(H2)/n(CO)=2:1的变化曲线;
答案:曲线b H2的含量越低,CO的转化率越低
(3) a.催化剂参与相关化学反应,但化学反应前后,催化剂的质量和化学性质不变,故a不正确;
b.在恒温恒压的平衡体系中充入氩气,体积增大,平衡逆向移动,CH3OH的产率降低,故b正确;
c.当2v(CO)正=v(H2)逆时,反应达到平衡状态,故c正确;
答案:bc
(4)设一氧化碳的反应量为x,根据甲
CO(g)+ 2H2(g)![]() CH3OH(g)
CH3OH(g)
n(初)2mol 6mol 0mol
△n xmol 2xmol xmol
n(平)(2-x)mol (6-2x)mol xmol
根据![]() =
=![]() ,得x=1,则容器的容积为2L,平衡后c(CO)=0.5mol/L,c(H2)=2mol/L,c(CH3OH)=0.5mol/L,则K=
,得x=1,则容器的容积为2L,平衡后c(CO)=0.5mol/L,c(H2)=2mol/L,c(CH3OH)=0.5mol/L,则K=![]() =
=![]() 或0.25;要使平衡后乙容器与甲容器中相同组分的体积分数相等,甲、乙必为等效平衡,因为起始时要维持化学反应向逆反应方向进行,可以根据平衡时甲醇的物质的量为1mol,确定c的物质的量大于1;根据假设甲容器反应进行到底生成甲醇2mol,确定c的物质的量小于2,得出乙容器中c的取值范围为1<c<2;
或0.25;要使平衡后乙容器与甲容器中相同组分的体积分数相等,甲、乙必为等效平衡,因为起始时要维持化学反应向逆反应方向进行,可以根据平衡时甲醇的物质的量为1mol,确定c的物质的量大于1;根据假设甲容器反应进行到底生成甲醇2mol,确定c的物质的量小于2,得出乙容器中c的取值范围为1<c<2;
答案:![]() 或0.25 1<c<2
或0.25 1<c<2
(5)①由于电解质为金属氧化物,则负极CO发生氧化反应与O2-结合生成CO2,电极反应式为:CO+O2--2e-=CO2
②阳极氧化失电子,电极反应式为2CH3OH+CO-2e-= (CH3O)2CO+2H+;
答案:CO+O2--2e-=CO2 2CH3OH+CO-2e-= (CH3O)2CO+2H+