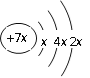题目内容
【题目】氮及其化合物在生产、生活和科技等方面有重要的应用。请回答下列问题:
(1)氮元素基态原子的价电子排布图为______________。
(2)在氮分子中,氮原子之间存在着______个σ键和______个π键。
(3)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3﹣,请写出两种与N3﹣互为等电子体的分子_______ 、_______。
(4)氮元素的氢化物(NH3)是一种易液化的气体,请阐述原因是_____________________。
(5)NF3、NCl3、NBr3的沸点由高到低的顺序是___________________________。
(6)Mg3N2遇水发生剧烈反应,生成一种有刺激性气味的气体.该反应的化学方程式为_______。
【答案】 ![]() 1 2 CO2 N2O 氨分子之间容易形成氢键,使其沸点升高而容易液化 NF3>NBr3>NCl3 Mg3N2+3H2O = 2NH3↑+3MgO。
1 2 CO2 N2O 氨分子之间容易形成氢键,使其沸点升高而容易液化 NF3>NBr3>NCl3 Mg3N2+3H2O = 2NH3↑+3MgO。
【解析】试题分析:本题通过N元素应用实例,主要考查价电子排图、共价键的类型、等电子体、氢键、分子晶体沸点的影响因素、化学方程式等知识,考查考生阅读方希能力和基础知识的综合应用能力。
解析:N元素核外电子排布式为1s22s22p3,价电子排布为2s22p3,价电子排布图为![]() 。正确答案:
。正确答案:![]() 。(2)N2分子结构式为N≡N,其中含有1个σ键,2个π键。正确答案:1、2。(3)N3-含有3个原子,价电子数为22,原子数目不变时,原子电子总数增加1,可以将1个N原子变成O原子,所以等电子体是N2O,同理,如果再将1个N原子换成C原子,必须同时将1个N原子换成O原子,所以等电子体也可以是CO2。正确答案:CO2、N2O。(4)NH3分子间存在氢键,沸点更高,所以NH3易液化。正确答案:氨分子之间容易形成氢键,使其沸点升高而容易液化。(5)NF3、NCl3、NBr3形成的晶体都是分子晶体,分子间只存在范德华力,按照NBr3、NCl3、NF3排序,随着相对分子质量的增大,分子间的范德华力增大,沸点升高,正确答案: NBr3>NCl3>NF3(6)Mg3N2遇水生成的有刺激性气味的气体是NH3,既N3-离子结合H+形成NH3,则Mg2+结合OH-形成Mg(OH)2。反应的化学方程式为Mg3N2+3H2O = 2NH3↑+3MgO。正确答案:Mg3N2+3H2O = 2NH3↑+3MgO。
。(2)N2分子结构式为N≡N,其中含有1个σ键,2个π键。正确答案:1、2。(3)N3-含有3个原子,价电子数为22,原子数目不变时,原子电子总数增加1,可以将1个N原子变成O原子,所以等电子体是N2O,同理,如果再将1个N原子换成C原子,必须同时将1个N原子换成O原子,所以等电子体也可以是CO2。正确答案:CO2、N2O。(4)NH3分子间存在氢键,沸点更高,所以NH3易液化。正确答案:氨分子之间容易形成氢键,使其沸点升高而容易液化。(5)NF3、NCl3、NBr3形成的晶体都是分子晶体,分子间只存在范德华力,按照NBr3、NCl3、NF3排序,随着相对分子质量的增大,分子间的范德华力增大,沸点升高,正确答案: NBr3>NCl3>NF3(6)Mg3N2遇水生成的有刺激性气味的气体是NH3,既N3-离子结合H+形成NH3,则Mg2+结合OH-形成Mg(OH)2。反应的化学方程式为Mg3N2+3H2O = 2NH3↑+3MgO。正确答案:Mg3N2+3H2O = 2NH3↑+3MgO。

【题目】几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是( )
元素代号 | A | B | D | E | X | Y | Z | W |
化合价 | -1 | -2 | +4、-4 | -1 | +5、-3 | +3 | +2 | +1 |
原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
A. A的单质能将E单质从YE3的溶液中置换出来
B. A、Y、W的离子半径由大到小顺序是A>W>Y
C. X元素的单质不存在同素异形体
D. Z在DB2中燃烧生成两种化合物
【题目】有关化学键的键能(指将1mol气态分子拆开形成气态原子时,每个化学键断裂所需的最低能量)数据如表所示:
化学键 | C-H | C=C | H-H | C-C |
键能/(KJ/mol) | 413.4 | x | 436.0 | 347.7 |
已知CH2=CH2(g)+H2(g)![]() CH3CH3(g) ΔH=-123.5kJ/mol,x的值为
CH3CH3(g) ΔH=-123.5kJ/mol,x的值为
A. 136.8 B. 307.5 C. 615.0 D. 177.3