题目内容
在一定温度下,体积固定的密闭容器中进行可逆反应A(g)+3B(g)?2C(g),下列关于该反应达到平衡状态的标志的说法中不正确的是( )
| A、单位时间内生成n mol A,同时生成3n mol B |
| B、A、B、C的浓度不再发生变化 |
| C、混合气体的压强不再发生改变 |
| D、C生成的速率与C分解的速率相等 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、单位时间内生成n mol A,同时生成3n mol B,从反应一开始,就有这个等量关系,故A错误;
B、A、B、C的浓度不再发生变化,正逆反应速率相等,达平衡状态,故B正确;
C、混合气体的压强不再发生改变,说明气体的总物质的量不变,正逆反应速率相等,达平衡状态,故C正确;
D、C生成的速率与C分解的速率相等,正逆反应速率相等,达平衡状态,故D正确;
故选A.
B、A、B、C的浓度不再发生变化,正逆反应速率相等,达平衡状态,故B正确;
C、混合气体的压强不再发生改变,说明气体的总物质的量不变,正逆反应速率相等,达平衡状态,故C正确;
D、C生成的速率与C分解的速率相等,正逆反应速率相等,达平衡状态,故D正确;
故选A.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
下列有关说法正确的是( )
| A、用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物 |
| B、镀锌铁板是利用了牺牲阳极的阴极保护法来达到防止腐蚀的目的 |
| C、取一定量水垢加盐酸,生成能使澄清石灰水变浑浊的气体,说明水垢的主要成分为CaCO3、MgCO3 |
| D、已知Cu2O+2H+═Cu2++Cu+H2O,氢气还原氧化铜后所得红色固体能完全溶于稀硝酸,说明还原产物是铜 |
下列说法正确的是( )
| A、在“火柴头中氯元素的检验”实验中,摘下几根未燃过的火柴头,将其浸于水中,稍后取少量溶液于试管中,滴加硝酸银溶液和稀硝酸后,即可判断氯元素的存在 |
| B、蔗糖、淀粉、油脂及其水解产物均为非电解质 |
| C、向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| D、酒精能使蛋白质变性,可用于杀菌消毒 |
下列有关实验装置及用途叙述完全正确的是( )
A、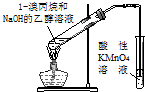 如图装置检验消去产物,中间应加水洗装置 |
B、 如图装置检验酸性:盐酸>碳酸>苯酚 |
C、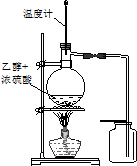 如图装置用于实验室制取并收集乙烯 |
D、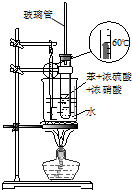 如图装置用于实验室制硝基苯 |
下列简单实验方案,不能实现实验目的是( )
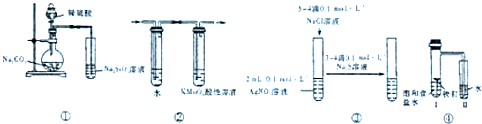

| A、①验证硫酸、碳酸、硅酸酸性强弱 |
| B、②检验溴乙烷发生消去反应生成的乙烯 |
| C、③验证AgCl沉淀能转化为溶解度更小的Ag2S沉淀 |
| D、④证明铁钉发生吸氧腐蚀 |
将0.2mol MnO2和50mL 12mol?L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量的AgNO3溶液,生成AgCl的物质的量为(不考虑盐酸的挥发)( )
| A、等于0.3 mol |
| B、小于0.3 mol |
| C、介于0.3~0.6 mol之间 |
| D、以上都不正确 |
下列物质的熔点高低顺序,正确的是( )
| A、金刚石>晶体硅>碳化硅 |
| B、K>Na>Li |
| C、NaF<NaCl<NaBr |
| D、CI4>CBr4>CCl4>CH4 |
 材料的不断发展可以促进社会进步.
材料的不断发展可以促进社会进步.