题目内容
下列有关实验装置及用途叙述完全正确的是( )
A、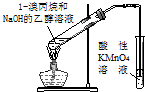 如图装置检验消去产物,中间应加水洗装置 |
B、 如图装置检验酸性:盐酸>碳酸>苯酚 |
C、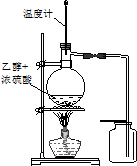 如图装置用于实验室制取并收集乙烯 |
D、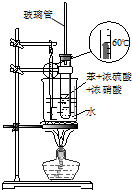 如图装置用于实验室制硝基苯 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.消去产物为乙烯,乙醇易挥发,且乙醇、乙烯均能被高锰酸钾氧化;
B.发生强酸制取弱酸的反应,但浓盐酸易挥发;
C.制备乙烯在170℃,且乙烯与空气密度相近;
D.苯与浓硝酸、浓硫酸加热制硝基苯,水浴加热.
B.发生强酸制取弱酸的反应,但浓盐酸易挥发;
C.制备乙烯在170℃,且乙烯与空气密度相近;
D.苯与浓硝酸、浓硫酸加热制硝基苯,水浴加热.
解答:
解:A.消去产物为乙烯,乙醇易挥发,且乙醇、乙烯均能被高锰酸钾氧化,则装置检验消去产物,中间应加水洗装置排除乙醇的干扰,故A正确;
B.发生强酸制取弱酸的反应,但浓盐酸易挥发,则装置检验酸性:盐酸>碳酸,不能确定碳酸>苯酚,盐酸也与苯酚钠反应,故B错误;
C.制备乙烯在170℃,且乙烯与空气密度相近,则温度计的水银球应在液面以下,最后利用排水法收集,故C错误;
D.苯与浓硝酸、浓硫酸加热制硝基苯,水浴加热,图中制备实验装置合理,故D正确;
故选AD.
B.发生强酸制取弱酸的反应,但浓盐酸易挥发,则装置检验酸性:盐酸>碳酸,不能确定碳酸>苯酚,盐酸也与苯酚钠反应,故B错误;
C.制备乙烯在170℃,且乙烯与空气密度相近,则温度计的水银球应在液面以下,最后利用排水法收集,故C错误;
D.苯与浓硝酸、浓硫酸加热制硝基苯,水浴加热,图中制备实验装置合理,故D正确;
故选AD.
点评:本题考查化学实验方案的评价,侧重于物质的性质、制备、酸性比较等实验方案的评价,注意把握相关物质的性质,为解答该类题目的关键,题目难度不大.

练习册系列答案
相关题目
用下列实验装置进行相应实验,不能达到实验目的是( )
A、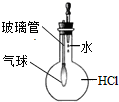 验证HCl极易溶于水 |
B、 石油分馏 |
C、 电解精炼铜 |
D、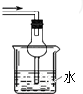 吸收氨气 |
在一定温度下,体积固定的密闭容器中进行可逆反应A(g)+3B(g)?2C(g),下列关于该反应达到平衡状态的标志的说法中不正确的是( )
| A、单位时间内生成n mol A,同时生成3n mol B |
| B、A、B、C的浓度不再发生变化 |
| C、混合气体的压强不再发生改变 |
| D、C生成的速率与C分解的速率相等 |
“化学是人类进步的关键”.下列说法不正确的是( )
| A、PM2.5是指空气中直径≤2.5μm的固体颗粒或液滴的总称 |
| B、根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子大小介于溶液与胶体之间 |
| C、科学家发现一种新细菌的DNA链中有砷(As)元素,该As元素最有可能取代了普通DNA链中的P元素 |
D、 和CO2反应生成可降解聚合物 和CO2反应生成可降解聚合物 ,该反应符合绿色化学的原则 ,该反应符合绿色化学的原则 |
根据下列物质的化学性质,判断其应用错误的是( )
| A、高纯度的硅单质广泛用于制作光导纤维 |
| B、CaO能与SO2反应,可作工业废气的脱硫剂 |
| C、明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| D、酒精能使蛋白质变性,可用于杀菌消毒 |
在一定温度下,可逆反应A(气)+3B(气)?2C(气)达到平衡的标志是( )
| A、C生成的速率与C分解的速率相等 |
| B、A、B、C的浓度相等 |
| C、A、B、C的分子数比为1:3:2 |
| D、单位时间生成n mol A,同时生成3n mol B |
下列反应中,能量变化不符合如图图示的是( )
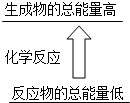

| A、酸与碱的中和反应 |
| B、煅烧石灰石制生石灰 |
| C、Ba(OH)2?8H2O与NH4Cl晶体反应 |
| D、焦炭与水蒸气反应 |
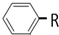 可以被KMnO4酸性溶液氧化成
可以被KMnO4酸性溶液氧化成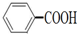 ,但若烷基R中直接与苯环相连的碳原子上没有C-H键,则不易被氧化得到
,但若烷基R中直接与苯环相连的碳原子上没有C-H键,则不易被氧化得到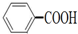 .现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成
.现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成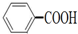 的异构体共有7种,其中两种是
的异构体共有7种,其中两种是 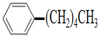 、
、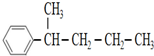 .请写出其他5种的结构简式:
.请写出其他5种的结构简式: