题目内容
4.下列说法正确的是( )| A. | 溶液是呈电中性的,而胶体是可以带电的 | |
| B. | 向沸水中加入FeCl3饱和溶液,继续煮沸至溶液呈红褐色时即得到Fe(OH)3胶体 | |
| C. | 清晨,阳光透过树叶间的缝隙可以产生丁达尔效应,说明空气是一种胶体 | |
| D. | 常用于区分溶液和胶体的方法是利用丁达尔效应,属于化学方法 |
分析 A.胶体是电中性的;
B.将饱和三氯化铁溶液滴人沸蒸馏水中来制取氢氧化铁胶体;
C.空气中的灰尘能形成胶体;
D.是否有新物质生成,是区分物理变化和化学变化的依据.
解答 解:A.溶液是电中性的,胶体也是电中性的,胶体粒子吸附了带电的离子,故A错误;
B.用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,然后将饱和三氯化铁溶液滴入沸水中,并继续煮沸至液体呈透明的红褐色即得氢氧化铁胶体,故B正确;
C.空气中的灰尘能形成胶体,空气不是胶体,故C错误;
D.丁达尔效应没有新物质生成,属于物理变化,故D错误.
故选B.
点评 本题考查胶体的重要性质,难度不大,注意溶液是电中性的,胶体也是电中性的,胶体粒子吸附了带电的离子.

练习册系列答案
相关题目
11.下列装置能达到相应实验目的是( )
| A. |  | B. | 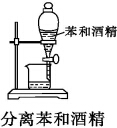 | C. |  | D. | 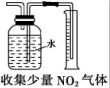 |
12.下列离子方程式正确的是( )
| A. | 铜与硝酸银溶液反应 Cu+Ag+═Cu2++Ag | |
| B. | CH3COOH溶液与NaOH溶液反应 H++OH-═H2O | |
| C. | 碳酸镁与稀H2SO4反应 MgCO3+2H+═Mg2++H2O+CO2↑ | |
| D. | 石灰乳与稀盐酸反应 H++OH-═H2O |
19.在某无色透明的溶液中,能大量共存的离子组是( )
| A. | H+、Na+、SO42-、HCO3-? | B. | Mg2+、K+、SO42-、OH- | ||
| C. | K+、Na+、Fe3+、NO3- | D. | Ba2+、OH-、NO3-、Na+ |
9.50g质量分数为19%的氧化镁溶液中Cl-的物质的量为( )
| A. | 0.01mol | B. | 0.1mol | C. | 0.02mol | D. | 0.2mol |
14.下列关于反应能量的说法正确的是( )
| A. | Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H=-216 kJ•mol-1,则反应物总能量大于生成物总能量 | |
| B. | 相同条件下,如果1 mol氢原子所具有的能量为E1,1 mol氢分子所具有的能量为E2,则2E1=E2 | |
| C. | 101 kPa时,2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2的燃烧热为571.6 kJ•mol-1 | |
| D. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则含1 mol NaOH的氢氧化钠固体与含0.5 mol H2SO4的稀硫酸混合后放出57.3 kJ的热量 |
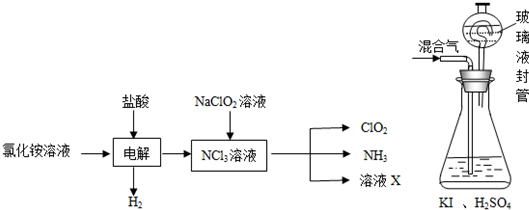
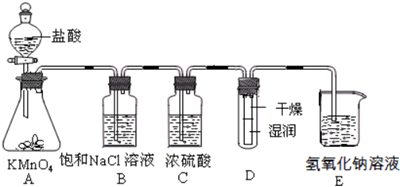
 .
.