��Ŀ����
5�������ϡ��ķ��ֺ�ʹ�������Ἣ����ƶ�����������ķ�չ��һЩ���ϵij�������������̱�ʽ��ʱ�������壮��ش��������⣺��1�����ǽ������ϣ��ߴ��ȵ������ǵ��͵����ǽ������ϣ��ֳơ��뵼�塱���ϣ����ķ��ֺ�ʹ��������������һ���������������ֲ��Ͽ������з����Ʊ���
SiO2$��_{����}^{��C}$Si���֣�$��_{300��}^{��HCl}$SiHCl3$��_{1000��1100��}^{������H_{2}}$Si������
��д������I�Ļ�ѧ����ʽ��SiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO����
�ڲ���������õ���SiHCl3���е�Ϊ33.0�棩�к���������SiCl4���е�Ϊ57.6�棩��HCl���е�Ϊ-84.7�棩���ᴿSiHCl3��ʵ�鷽������������
�������йع���ϵ�˵����ȷ����AD
A�����ʹ軯ѧ�����ȶ��������Ա�ǿ����Һ��ʴ
B�����������跴Ӧ���ʲ�������Ϊ��Һ�ⵥ����
C����ͨ�������ɴ��ʯ��ʯ��ʯӢɰ�Ƴɵģ����۵�ܸ�
D�����ά����Ҫ�ɷ���SiO2
�������������ܵ�����ʱ����Ҫʹ��һ���������ǽ���������ֲ�����ڣ����ֲ�����B������ĸ����
A�����½ṹ�մ� ��B�������մɡ� C�������մ�
��2���������ϣ�����������ָ����Ԫ�ػ��Խ���Ԫ��Ϊ�����ɵľ��н������ԵIJ��ϵ�ͳ�ƣ��������������Ͻ�����ֽ������ϵȣ����������в����ںϽ����D
A������ B����ͭ C��Ӳ�� D��ˮ��
��3���߷��Ӳ��ϣ������Էֳ����߷��Ӳ��Ϻ��л��߷��Ӳ��ϣ�[Al Fe ��OH��nCl6-n]m�������߷��Ӳ��ϣ���һ������Ч��ˮ�������㷺Ӧ��������ˮ��ҵ��ˮ�Ĵ�����������Ԫ�صĻ��ϼ�Ϊ+3��
��4�����Բ��ϣ�ij���Է�ĩ������һ�ָ����������Ϊ�ⶨ����ɣ��ֳ�ȡ6.26g��Ʒ������ȫ�����ڹ���ϡHNO3���������Na2SO4��Һ������4.66g��ɫ���������ˣ�����Һ�м������NaOH��Һ�����ɺ��ɫ���������������ˡ�ϴ�ӡ����պ��3.20g���壮�ٸô��Է�ĩ����Ԫ�ص���������Ϊ20.45%���ڸò��ϵĻ�ѧʽΪBaO•Fe2O3��
���� ��1���ٽ�̿�ڸ����¿����û����������еĹ裻
�ڸ����۷е�IJ�ͬʵ�����ʷ���ķ���Ϊ��������
��A�������������Ʒ�Ӧ���ɹ����ƺ�������
B�����������Ӧ��
C������Ϊ���������ڹ̶����۵㣻
D����������Ϊ���ά����Ҫ�ɷ֣�
�������������ٵ��մɣ�Ӧ�������õ��������ܣ��ݴ˷�����
��2�����ݺϽ��ǽ����ͽ�����ǽ����γɵľ��л�ѧ���Ե����ʣ����������ɺͺϽ�ĸ�������жϣ�
��3������AlFe��OH��nCl6-n�и�Ԫ�صĻ��ϼ۴�����Ϊ0������Ԫ�صĻ��ϼۣ�
��4�����������Ϣ��֪���ɵij���Ϊ���ᱵ������õ���Ԫ�����ʵ���������Һ�м������NaOH��Һ�����ɺ��ɫ���������������ˡ�ϴ�ӡ����պ��3.20g���壬������Ӧ���̿�֪Ϊ������������õ���Ԫ�����ʵ������������������Ԫ�ؾ���������Ԫ�������õ��������������ݼ���õ���Ԫ�ء���Ԫ�ء���Ԫ�����ʵ�������õ�������Ļ�ѧʽ��
��� �⣺��1���ٹ�ҵ���ý�̿�ڸ������û����������еĹ����Ʊ��ֹ裬����ʽΪ��SiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO����
�ʴ�Ϊ��SiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO����
��SiHCl3���е�33.0�棩��SiCl4���е�57.6�棩��HCl���е�-84.7�棩�����ǵķе㲻ͬ�����ݷе�IJ�ͬʵ�����ʷ���ķ���Ϊ��������
�ʴ�Ϊ����������
��A�������������Ʒ�Ӧ���ɹ����ƺ����������Ա�ǿ����Һ��ʴ����A��ȷ��
B�����������Ӧ����B����
C������Ϊ���������ڹ̶����۵㣬��C����
D����������Ϊ���ά����Ҫ�ɷ֣���D��ȷ��
�ʴ�Ϊ��AD��
�������������ٵ��մɣ�Ӧ�������õ��������ܣ�
�ʴ�Ϊ��B��
��2��A��Ӳ������Al��Cu��Mg��Mn��Si���γɵĺϽ𣬹�A�����ϣ�
B����ͭ��Cu��Zn�ĺϽ𣬹�B�����ϣ�
C������������̼���γɵĺϽ𣬹�C�����ϣ�
D��ˮ���ǽ����������ڽ������ʣ����ǺϽ𣬹�D���ϣ�
�ʴ�Ϊ��D��
��3��������[Al Fe ��OH��nCl6-n]m����Ԫ����+3�ۣ�������Ϊ-1�ۣ���Ԫ�صĻ��ϼ۴�����Ϊ0������Ԫ�صĻ��ϼ�Ϊ+3�ۣ�
�ʴ�Ϊ��+3��
��4����n��BaSO4��=$\frac{4.66g}{233g/mol}$=0.02mol��m��Ba��=137g/mol��0.02mol=2.74g����Һ�м����������������Һ�����ɺ��ɫ����Ϊ��������������ϴ�����յõ�3.20g����Ϊ����������n��Fe2O3��$\frac{3.20g}{160g/mol}$=0.02mol��m��Fe��=0.04mol��56g/mol=2.24g����������������Ԫ�ص�����=6.26g-2.74g-2.24g=1.28g������Ԫ����������=$\frac{1.28g}{6.26g}$��100%=20.45%��
�ʴ�Ϊ��20.45%��
��1.28g��Ԫ�ص����ʵ���=$\frac{1.28g}{16g/mol}$=0.08mol���ɢټ����֪�������������б�ԭ�ӡ���ԭ�ӡ���ԭ�ӵ����ʵ���֮��=0.02��0.02��2��0.08=1��2��4��
����ԭ����֮��Ϊ1��2��4����ѧʽΪBaO•Fe2O3��
�ʴ�Ϊ��BaO•Fe2O3��
���� ���⿼���˹輰�仯��������ʺ���;���������ʵķ���Ӧ�ã��Ͻ���������Ӧ�õ�֪ʶ�����ӻ�ѧʽ�ļ��㷽���ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | I- | B�� | I2 | C�� | I2+ | D�� | I${\;}_{3}^{-}$ |
| A�� | B2Ϊ0.1mol/L | B�� | DΪ0.3mol/L | ||
| C�� | A2Ϊ0.3mol/L | D�� | B2Ϊ0.2mol/LͬʱDΪ0.1mol/L |
 ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�
ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�CH3CH2OH $��_{170��}^{Ũ����}$CH2=CH2��+H2O
CH2=CH2+Br2��BrCH2CH2Br
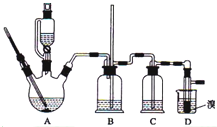
���ܴ��ڵ���Ҫ����Ӧ�У��Ҵ���Ũ����Ĵ�������l40����ˮ�������ѣ�������������������Ҵ��Ʊ�1��2-���������װ����ͼ��ʾ���й������б����£�
| �Ҵ� | 1��2-�������� | ���� | |
| ״̬���ܽ��� | ��ɫҺ�塢������ˮ | ��ɫҺ�� | ��ɫҺ�塢������ˮ |
| �ܶ�/g•cm-3 | 0.79 | 2.2 | 0.71 |
| �е�/�� | 78.5 | 132 | 34.6 |
| �۵�/�� | -l30 | 9 | -1l6 |
��1���ڴ��Ʊ�ʵ���У�Ҫ������Ѹ�ٵذѷ�Ӧ�¶����170�����ң�������ҪĿ����d��
a��������Ӧ b���ӿ췴Ӧ�ٶ� c����ֹ�Ҵ��ӷ� d�����ٸ�������������
��2���жϸ��Ʊ���Ӧ�Ѿ�������������������ɫ��ȫ��ȥ��
��3����1��2-��������ֲ�Ʒ���ڷ�Һ©���м�ˮ�����ã�����Ӧ�ڲ��£���ϡ������¡�����
��4�������������������������ѣ����õķ�����ȥ����
��5����Ӧ������Ӧ����ˮ��ȴװ��D������ҪĿ���ǣ����ֲ��ܹ�����ȴ�����ñ�ˮ������ԭ���DZ���������ӷ�����Ʒ1��2-����������۵㣨���̵㣩�ͣ�������ȴ�����̶��������ܣ�
 S2Cl2�ǹ�ҵ�ϳ��õ��������Ըı��������ȷ�ճ�������Ӳ�����ʣ�
S2Cl2�ǹ�ҵ�ϳ��õ��������Ըı��������ȷ�ճ�������Ӳ�����ʣ�| ���� | �е�/�� | �۵�/�� |
| S | 445 | 113 |
| CS2 | 47 | -109 |
| CCl4 | 77 | -23 |
| S2Cl2 | 137 | -77 |
ʵ�����Ʊ�S2Cl2�ķ�Ӧԭ�������֣�
��CS2+3C12$\frac{\underline{\;95��100��\;}}{\;}$ CC14+S2Cl2��
��2S+Cl2$\frac{\underline{\;111��140��\;}}{\;}$ S2Cl2��
��1����ʵ����ѡ��ͼװ�ã����ּг�װ������ȥ�����Ʊ�S2Cl2���䷴Ӧԭ���������еĢ٣���д��ţ���ͼ��β������װ�ò������ƣ��Ľ����װ��Ӧ�������ǣ���D��E֮������װ�������β�����ա������������ã����øĽ������ȷװ�ý���ʵ�飬��ش��������⣺
��2��Ϊ����߲�ƷS2Cl2�Ĵ��ȣ�ʵ������Ĺؼ��ǿ��ƺ��¶ȺͿ���Ũ����ĵ��ٲ�Ҫ̫�죮
��3����ʵ��IJ���˳��Ϊ���٢ۢڢݢܣ�����ű�ʾ����
�ٵ�ȼ�ƾ���A �ڵ�ȼ�ƾ���D ��ͨ����ˮ ��Ϩ��ƾ���A ��Ϩ��ƾ���D
��4��ijͬѧȡ�������С�ļ�������ˮ�У��۲쵽�а�������ɫ�����Ҳ�������ɫ������ʹƷ����Һ��ɫ����ͬѧ�ݴ��ж�����ʵ��ȷ��S2Cl2���ɣ�д��S2Cl2��ˮ��Ӧ�Ļ�ѧ����ʽ��2S2Cl2+2H2O�T3S��+SO2��+4HCl����
��5��S2Cl2��ÿ��ԭ�ӵ�����㶼����8���ӽṹ�����õ���ʽ��ʾS2Cl2���γɹ��̣�
 ��
�� | A�� | ������ | B�� | ���� | C�� | ��ˮ | D�� | ���� |
| A�� | �ɲ�ͬԪ����ɵĹ��ۻ�������һ��ֻ���ڼ��Լ� | |
| B�� | �����ԭ���У�����˽�Զ���������˶��ĵ��������ϵ� | |
| C�� | ��ѧ���ڹ���Ԫ����Ѱ�Ҵ��������¡���ʴ�ĺϽ���� | |
| D�� | ������ѧ��Ӧ�������������Ƿų��������Ƿ�Ӧ���������Ķ��� |

