题目内容
2.下列离子方程式与所述事实相符且正确的是( )| A. | 向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2═4Fe3++6Cl-+Br2 | |
| B. | 磁性氧化铁溶于氢碘酸:Fe3O4+8H+═2Fe3++Fe2++4H2O | |
| C. | 放置在空气中的淀粉碘化钾溶液一段时间后溶液呈蓝色:4H++4I-+O2═2I2+2H2O | |
| D. | 向硝酸铵溶液中滴加NaOH溶液:NH4++OH-═NH3↑+H2O |
分析 A.亚铁离子的还原性大于溴离子,氯气不足时亚铁离子优先反应,剩余的氯气再与溴离子反应,据此根据反应物过量情况分析反应产物;
B.铁离子具有氧化性,能够将碘离子氧化成碘单质,反应后的溶液中不会存在铁离子;
C.碘离子被空气中氧气氧化成碘单质;
D.铵根离子与氢氧根离子反应生成一水合氨.
解答 解:A.向含有0.4 mol FeBr2的溶液中含有0.4mol亚铁离子、0.8mol溴离子,0.4mol亚铁离子完全反应消耗0.2mol氯气,剩余的0.1mol氯气能够氧化0.2mol溴离子,则参加反应的亚铁离子与溴离子的物质的量之比为2:1,该反应的离子方程式为:4Fe2++2Br-+3Cl2═4Fe3++6Cl-+Br2,故A正确;
B.磁性氧化铁溶于氢碘酸,二者发生氧化还原反应,正确的离子方程式为:2I-+Fe3O4+8H+=3Fe2++4H2O+I2,故B错误;
C.放置在空气中的淀粉碘化钾溶液一段时间后溶液呈蓝色,反应的离子方程式为:4H++4I-+O2═2I2+2H2O,故C正确;
D.硝酸铵溶液中滴加NaOH溶液,反应生成一水合氨,正确的离子方程式为:NH4++OH-═NH3•H2O,故D错误;
故选AC.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.下列叙述正确的是( )
| A. | 3.01×1023个SO2分子的质量为32g | B. | CH4的摩尔质量为16g | ||
| C. | 1molH2O的质量为18g/mol | D. | O的摩尔质量是32g/mol |
13.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:
下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2 min的平均速率v(Z)=2.0×10-3 mol/(L•min) | |
| B. | 该温度下此反应的平衡常数K=144 | |
| C. | 其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变 | |
| D. | 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正) |
10.下列物质互为同分异构体的是( )
| A. | 2-甲基丁烷和异戊烷 | B. | 分子量相同而结构不同的两种物质 | ||
| C. |  和 和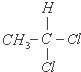 | D. | 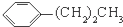 和 和 |
17.在Na2O2与H2O反应中,发生氧化反应和还原反应得物质的量之比是( )
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 8:53 |
7.相同温度下,根据三种酸的电离常数,下列判断正确的是( )
| 酸 | HX | HY | HZ |
| 电离常数K | 9×10-7 | 9×10-6 | 10-2 |
| A. | 三种酸的强弱关系:HX>HY>HZ | |
| B. | 反应HZ+Y-═HY+Z-能够发生 | |
| C. | 相同温度下,0.1 mol•L-1的HX、HY、HZ溶液,HX与锌反应一定最快 | |
| D. | 相同温度下,1 mol•L-1 HX溶液的电离常数大于0.1 mol•L-1 HX |
14.在给5mL某液体加热的操作中,下列仪器一定不需要的是( )
| A. | 试管 | B. | 酒精灯 | C. | 试管夹 | D. | 集气瓶 |
11.下列溶液中的氯离子数目与50mL 1mol•L-1的FeCl3溶液中氯离子数目相等( )
| A. | 50 mL 1.5 mol•L-1的FeCl2溶液 | B. | 100 mL 3 mol•L-1的NH4Cl溶液 | ||
| C. | 75 mL 3 mol•L-1的KCl溶液 | D. | 50 mL 2 mol•L-1的CaCl2溶液 |
12.下列物质性质与应用对应关系正确的是( )
| A. | 晶体硅熔点高硬度大,可用于制作半导体材料 | |
| B. | 氢氧化铝胶体具有吸附性,可用于制胃酸中和剂 | |
| C. | 漂白粉在空气中不稳定,可用于漂白纸张 | |
| D. | 氧化铁呈红棕色,可用于制作红色涂料 |