题目内容
11.下列关于HC≡C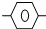 CH2-CH=CHCH3的说法正确的是( )
CH2-CH=CHCH3的说法正确的是( )| A. | 所有C原子可能共平面 | B. | 除苯环外的C原子共直线 | ||
| C. | 最多只有10个C共平面 | D. | 最多只有4个C共直线 |
分析 根据常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行共线、共面分析判断,注意单键可以旋转.
解答 解:A.碳碳单键可以旋转,乙炔与乙烯所在的平面一定共面,乙烯所在的平面与苯所在的平面可能在同一平面上,所以所有C原子可能共平面,故A正确;
B.苯是平面型结构,共线的原子共有4个,乙炔是直线型结构,共线的原子共有4个,乙烯是平面型结构,共线的原子共有2个,除苯环外的C原子不可能共直线,故B错误;
C.碳碳单键可以旋转,乙炔与乙烯所在的平面一定共面,乙烯所在的平面与苯所在的平面可能在同一平面上,所以所有C原子可能共平面,故C错误;
D.苯是平面型结构,共线的原子共有4个,乙炔是直线型结构,共线的原子共有4个,乙烯是平面型结构,共线的原子共有2个,最多只有5个C共直线,故D错误.
故选A.
点评 本题考查有机物的结构与性质,题目难度中等,注意掌握常见有机物结构与性质,合理分析该有机物分子中最多共平面的原子.

练习册系列答案
相关题目
1.将海水淡化与浓海水资源结合起来是综合利用海水的重要途径.
(1)先把浓海水中溴离子氧化成Br2,再利用“空气吹出法”从浓海水中吹出Br2,用纯碱来吸收,Br2又变成化合态溴,这样做的目的是使Br2富集.利用纯碱吸收溴单质的主要反应式是:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3则纯碱吸收了6molBr2时,转移的电子为10mol
(2)从浓海水中生产镁单质的一段工艺流程如图:
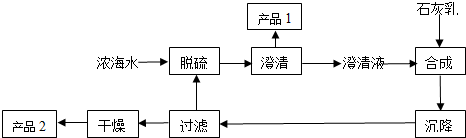
又知浓海水的主要成分如下表:
①该工艺过程中,产品1中一定含有的离子是钙离子和硫酸根离子,产品2的化学式为Mg(OH)2.
②1m3浓海水最多可得产品2的质量为69.60 kg.
(3)工业生产镁单质的化学方程式为MgCl2(熔融)$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
(4)从海水中提取出的氯化钠可用于氯碱工业,则氯碱工业主要反应原理的离子方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑.
(1)先把浓海水中溴离子氧化成Br2,再利用“空气吹出法”从浓海水中吹出Br2,用纯碱来吸收,Br2又变成化合态溴,这样做的目的是使Br2富集.利用纯碱吸收溴单质的主要反应式是:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3则纯碱吸收了6molBr2时,转移的电子为10mol
(2)从浓海水中生产镁单质的一段工艺流程如图:

又知浓海水的主要成分如下表:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g/L) | 63.7 | 28.8 | 144.6 | 46.4 |
②1m3浓海水最多可得产品2的质量为69.60 kg.
(3)工业生产镁单质的化学方程式为MgCl2(熔融)$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
(4)从海水中提取出的氯化钠可用于氯碱工业,则氯碱工业主要反应原理的离子方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑.
2.请选用适当的试剂和分离方法除去下列物质中所含的杂质(括号内为杂质),将所选的试剂及分离方法的编号填入表中.
试剂:a.H2O b.酸性KMnO4溶液 c.Br2的CCl4溶液 d.饱和Na2CO3溶液 e.新制CaO
分离方法:A.分液 B.过滤 C.洗气 D.蒸馏 E.盐析
试剂:a.H2O b.酸性KMnO4溶液 c.Br2的CCl4溶液 d.饱和Na2CO3溶液 e.新制CaO
分离方法:A.分液 B.过滤 C.洗气 D.蒸馏 E.盐析
| 混合物 | 选择试剂 | 分离方法 |
| 二氧化硫(乙烯) | c | C |
| 乙醇(水) | e | D |
| 乙酸乙酯(乙酸) | d | A |
19.下列物质在指定状态下的电离方程式正确的是( )
①水溶液 NaHSO4=Na++HSO4-②熔融状态 NaHSO4=Na++HSO4-
③水溶液中 NaHCO3=Na++HCO3-④水溶液 H3PO4?3H++PO43-
⑤水溶液 H2S+H2O?H3O++HS- ⑥水溶液 HF+H2O?H3O++F-.
①水溶液 NaHSO4=Na++HSO4-②熔融状态 NaHSO4=Na++HSO4-
③水溶液中 NaHCO3=Na++HCO3-④水溶液 H3PO4?3H++PO43-
⑤水溶液 H2S+H2O?H3O++HS- ⑥水溶液 HF+H2O?H3O++F-.
| A. | ④⑤⑥ | B. | ①③⑤ | C. | ②④⑥ | D. | ②③⑤⑥ |
6.若在一支试管中加入2mL的X溶液,然后再加入足量的氯水,再滴加几滴KSCN溶液,观察到溶液呈血红色,则X溶液中( )
| A. | 一定含有Fe3+ | B. | 一定不含Fe3+ | C. | 可能含有Fe2+ | D. | 一定含有Fe2+ |
16.下列物质中既含有共价键,又含有离子键的是( )
| A. | MgCl2 | B. | HClO | C. | Na2O | D. | KOH |
3.某混合溶液中含SO42-0.25mol/L,含Cl-0.5mol/L,NO3-0.25mol/L,含Na+0.25mol/L,其余为H+,则H+的物质的量浓度为( )
| A. | 5mol/L | B. | 2.5mol/L | C. | 1mol/L | D. | 0.1mol/L |
12.25℃时,将某一元碱MOH和盐酸溶液等体积混合(体积变 化忽略不计),测得反应后溶液的pH如下表,则下列判断不正确的是( )
| 实验编号 | c(盐酸)/(mol/L) | c(MOH)/(mol/L) | 反应后溶液的pH |
| 甲 | 0.20 | 0.20 | 5 |
| 乙 | 0.10 | a | 7 |
| A. | 实验甲所得溶液:c(Cl-)>c(M+)>c(H+)>c(MOH) | |
| B. | 将实验甲中所得溶液加水稀释后,$\frac{c({H}^{+})}{c({M}^{+})}$变小 | |
| C. | a>0.10 | |
| D. | MOH的电离平衡常数可以表示为Kb=$\frac{1{0}^{-8}}{a-0.10}$ |