题目内容
6.若在一支试管中加入2mL的X溶液,然后再加入足量的氯水,再滴加几滴KSCN溶液,观察到溶液呈血红色,则X溶液中( )| A. | 一定含有Fe3+ | B. | 一定不含Fe3+ | C. | 可能含有Fe2+ | D. | 一定含有Fe2+ |
分析 氯水能将Fe2+氧化为Fe3+,滴入KSCN溶液,观察到溶液呈血红色,则溶液中含Fe3+,而此时存在的Fe3+可能是原溶液本来就有的,也可能是原溶液中的Fe2+被氧化生成的,据此分析.
解答 解:由于氯水能将Fe2+氧化为Fe3+,故先加入足量的氯水后,再滴入KSCN溶液,观察到溶液呈血红色,则说明此时溶液中含Fe3+,而此时存在的Fe3+可能是原溶液本来就有的,也可能是原溶液中的Fe2+被氧化生成的,故原溶液中可能含Fe3+,也可能含Fe2+,故选C.
点评 本题考查物质的检验及鉴别,明确物质的性质是解答本题的关键,注意物质性质的差异即可解答,题目难度不大.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
16.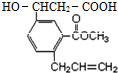 某有机物的结构简式如图所示,该有机物可能发生的反应是( )
某有机物的结构简式如图所示,该有机物可能发生的反应是( )
①酯化反应;②银镜反应;③加成反应;④取代反应;⑤氧化反应;⑥加聚反应;⑦缩聚反应;⑧水解反应.
 某有机物的结构简式如图所示,该有机物可能发生的反应是( )
某有机物的结构简式如图所示,该有机物可能发生的反应是( )①酯化反应;②银镜反应;③加成反应;④取代反应;⑤氧化反应;⑥加聚反应;⑦缩聚反应;⑧水解反应.
| A. | ①③④⑤⑥⑦⑧ | B. | ①②③④⑤⑥⑧ | C. | ①②③⑥⑧ | D. | ①③④⑤⑥⑧ |
17.蓄电池在放电时起原电池的作用,在充电时起电解池的作用.下面是爱迪生蓄电池分别在充电和放电时发生的反应:Fe+NiO2+2H2O$?_{充电}^{放电}$Fe(OH)2+Ni(OH),下列有关爱迪生蓄电池的推断错误的是( )
| A. | 放电时,Fe是负极,NiO2是正极 | |
| B. | 蓄电池的电极可以浸入某种碱性电解质溶液中 | |
| C. | 充电时,阴极上的电极反应为:Fe(OH)2+2e-=Fe+2OH- | |
| D. | 放电时,电解质溶液中的阴离子向正极方向移动 |
1.水的电离过程为H2O?H++OH-,在不同温度下其平衡常数为Kw(25℃)=1.0×10-14,Kw(35℃)=2.1×10-14.则下列叙述正确的是( )
| A. | 水的电离是一个放热过程 | |
| B. | 35℃时,c(H+)>c(OH-) | |
| C. | 25℃时,pH=3的盐酸中由水电离产生的c(OH-)=1.0×10-3mol/L | |
| D. | 25℃时,向溶液中加入稀氨水,平衡逆向移动,Kw不变 |
11.下列关于HC≡C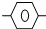 CH2-CH=CHCH3的说法正确的是( )
CH2-CH=CHCH3的说法正确的是( )
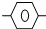 CH2-CH=CHCH3的说法正确的是( )
CH2-CH=CHCH3的说法正确的是( )| A. | 所有C原子可能共平面 | B. | 除苯环外的C原子共直线 | ||
| C. | 最多只有10个C共平面 | D. | 最多只有4个C共直线 |
18.下列离子式方程正确的是( )
| A. | 稀硝酸与氢氧化钡溶液反应:H++OH-═H2O | |
| B. | 铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 碳酸钠与稀硝酸反应:Na2CO3+2H+═2Na++CO2↑+H2O | |
| D. | 氯化铝溶液与过量氨水反应:Al3++OH-═Al(OH)3↓ |
7.从柑橘中炼制萜二烯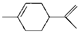 ,下列有关它的推测,不正确的是( )
,下列有关它的推测,不正确的是( )
 ,下列有关它的推测,不正确的是( )
,下列有关它的推测,不正确的是( )| A. | 分子式为C10 H16 | |
| B. | 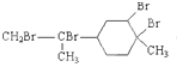 与过量的溴的CCl4溶液反应后产物如图 | |
| C. | 它不能使酸性高锰酸钾溶液褪色 | |
| D. | 常温下为液态,难溶于水 |

