题目内容
16.下列物质中既含有共价键,又含有离子键的是( )| A. | MgCl2 | B. | HClO | C. | Na2O | D. | KOH |
分析 一般金属元素与非金属元素形成离子键,非金属元素之间形成共价键,以此来解答.
解答 解:A.MgCl2只有镁离子与氯离子形成的离子键,故A错误;
B.HClO中氢原子和O原子之间存在共价键,O与Cl原子间存在共价键,故B错误;
C.Na2O中只有钠离子与氧离子形成的离子键,故C正确;
D.KOH中钾离子和氢氧根之间存在离子键,氢氧根离子中氧原子和氢原子之间存在共价键,故D正确;
故选:D.
点评 本题主要考查化学键,熟悉判断化学键的一般规律即可解答,题目难度不大.

练习册系列答案
相关题目
6.下列说法正确的是( )
| A. | SiO2 是酸性氧化物,能与氢氟酸反应 | |
| B. | Na2O、Na2O2组成元素相同,与 CO2反应产物也相同 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
7.设NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.00mol•L-1NaCl溶液中含有Na+的数目为NA | |
| B. | 常压下常温,6.4g由氧气和臭氧组成的混合物中含有的分子总数为0.2NA | |
| C. | 标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA | |
| D. | 7.8g过氧化钠含有的共用电子对数为0.1NA |
4.由于浓度不同而能发生不同氧化还原反应的是( )
| A. | Fe与H2SO4溶液 | B. | Fe与FeCl3溶液 | C. | Fe与HCl溶液 | D. | Fe与CuSO4 溶液 |
11.下列关于HC≡C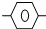 CH2-CH=CHCH3的说法正确的是( )
CH2-CH=CHCH3的说法正确的是( )
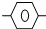 CH2-CH=CHCH3的说法正确的是( )
CH2-CH=CHCH3的说法正确的是( )| A. | 所有C原子可能共平面 | B. | 除苯环外的C原子共直线 | ||
| C. | 最多只有10个C共平面 | D. | 最多只有4个C共直线 |
1.25℃,相应条件下,下列各组离子一定能大量共存的是( )
| A. | c(H+)=1×10-13 mol•L-1的溶液中:Na+、Mg2+、I-、SO42- | |
| B. | 0.1mol•L-1的明矾溶液中:K+、NH4+、Cl-、HCO3- | |
| C. | pH=1的溶液中:Na+、NH4+、MnO4-、S2O32- | |
| D. | 无色透明的溶液中:Na+、Ba2+、Br-、NO3- |
5.按Si、P、S、Cl的顺序递减的是( )
| A. | 单质的氧化性 | B. | 得电子能力 | C. | 氢化物的稳定性 | D. | 原子半径 |