题目内容
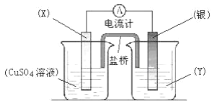
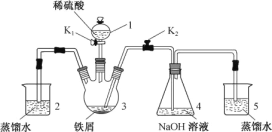
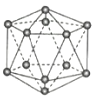
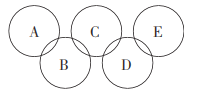
【题目】图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示:

回答下列问题:
(1)图B对应的物质名称是______,晶体类型为______。
(2)d中元素的原子核外电子排布式为 ______
(3)图A中由二种元素组成的物质中,沸点最高的是 ______,原因是______,该物质的分子构型为______。
(4)图A中的双原子分子中,极性最大的分子是______。
(5)k的分子式为______,中心原子的杂化轨道类型为______,属于______分子(填“极性”或“非极性”)。K又称光气,实验室制取时,可用四氯化碳与发烟硫酸(SO3的硫酸溶液)反应。将四氯化碳加热至55-60℃,滴加入发烟硫酸,即发生逸出光气和磺酰氯(该物质在高温时分解成SO2和Cl2),写出制取光气的化学方程式:______。
制取光气也可用氯仿和双氧水直接反应,生成光气和一种极易溶于水的气体,且水溶液呈强酸性,写出该化学方程式:______。
【答案】金刚石 原子晶体 1s22s22p63s23p5 H2O 分子间形成氢键 V形 HCl COCl2 sp2 极性 SO3+CCl4=SO2Cl2+COCl2↑ CHCl3+H2O2=HCl+H2O+COCl2
【解析】
a、b、c和d分别为四种短周期元素的常见单质,b与c反应生成水,则b、c分别为H2、O2中的一种,a的一种同素异形体的晶胞中每个原子周围有4个键,判断为金刚石,则a为C元素,则b为H2、c为O2,由转化关系可知,f为CO,g为CO2,因i是常见的酸,只由b、d形成可判断为盐酸,则d为Cl2,i为HCl,而k与水反应生成CO2与盐酸,该反应没在教材中出现过,且由f、d反应得到,应含C、O、Cl三种元素,只能判断为COCl2,据此解答。
根据上述分析可知:a是C,b是H2,c是O2,d为Cl2,f为CO,g为CO2,i为HCl,k为COCl2。
(1)根据上面的分析可知,图B对应的物质名称是金刚石,属于原子晶体;
(2)d中元素为Cl元素,基态原子电子排布式为1s22s22p63s23p5;
(3)在上所有两元素形成的物质中,只有水是液态,其它都是气体,故水的沸点最高,是由于在水分子之间除存在分子间作用力外,还有氢键,水分子中O原子形成2个σ键、含有2对孤电子对,杂化轨道数目为4,产生sp3杂化,所以分子构型为V形;
(4)在上述元素形成的所有双原子分子中,只有H、Cl电负性差值最大,因而HCl的极性最大;
(5)k的分子式为COCl2,COCl2中C原子成3个σ键、1个π键,没有孤电子对,C原子采取sp2杂化,分子中正负电荷中心不重合,属于极性分子,四氯化碳与发烟硫酸(SO3的硫酸溶液)反应,制取光气的化学方程式为SO3+CCl4═SO2Cl2+COCl2↑.制取光气也可用氯仿和双氧水直接反应,生成光气和一种极易溶于水的气体,且水溶液呈强酸性,其化学方程式为CHCl3+H2O2=HCl+H2O+COCl2。

 53随堂测系列答案
53随堂测系列答案【题目】观察下列模型并结合有关信息,判断下列说法不正确的是( )
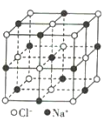
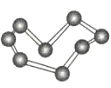
晶体硼(其每个结构单元中有12个B原子) | NaCl | S8 | HCN | |
结构模型示意图 |
|
|
|
|
备注 | 熔点2573K | —— | 易溶于CS2 | —— |
A.晶体硼属于原子晶体,结构单元中含有30个B-B键,含20个正三角形
B.NaCl晶体中每个Na+周围距离最近且相等的Na+有6个
C.S8分子中的共价键为非极性键
D.HCN分子中含有2个σ键,2个π键