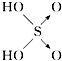题目内容
【题目】判断含氧酸强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强.含氧酸酸性强弱与非羟基氧原子数的关系如表所示:
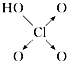
含氧酸 | 次氯酸 | 磷酸 | 硫酸 | 高氯酸 |
结构式 | Cl﹣OH |
|
|
|
非羟基氧原子数 | 0 | 1 | 2 | 3 |
酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
已知:亚磷酸(H3PO3)和亚砷酸(H3AsO3)分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性.由此可推出:
①H3PO3的结构式为 , H3PO3与过量的NaOH溶液反应的化学方程式为;
②H3AsO3的结构式为 , 在H3AsO3中加入浓盐酸,反应的化学方程式为 .
【答案】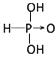 ;H3PO3+2NaOH=Na2HPO3+2H2O;
;H3PO3+2NaOH=Na2HPO3+2H2O;![]() ;As(OH)3+3HCl=AsCl3+3H3O
;As(OH)3+3HCl=AsCl3+3H3O
【解析】解:①含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强,亚磷酸是中强酸,所以亚磷酸的结构式为  ;H3PO3与过量的NaOH溶液反应的化学方程式为 H3PO3+2NaOH=Na2HPO3+2H2O,所以答案是:
;H3PO3与过量的NaOH溶液反应的化学方程式为 H3PO3+2NaOH=Na2HPO3+2H2O,所以答案是:  ; H3PO3+2NaOH=Na2HPO3+2H2O;②亚砷酸既有弱酸性又有弱碱性,所以亚砷酸的结构式为
; H3PO3+2NaOH=Na2HPO3+2H2O;②亚砷酸既有弱酸性又有弱碱性,所以亚砷酸的结构式为 ![]() ,亚砷酸和盐酸能反应,反应方程式为As(OH)3+3HCl=AsCl3+3H3O,所以答案是:
,亚砷酸和盐酸能反应,反应方程式为As(OH)3+3HCl=AsCl3+3H3O,所以答案是: ![]() ;As(OH)3+3HCl=AsCl3+3H3O.
;As(OH)3+3HCl=AsCl3+3H3O.
【考点精析】根据题目的已知条件,利用弱电解质在水溶液中的电离平衡的相关知识可以得到问题的答案,需要掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.

练习册系列答案
相关题目