题目内容
【题目】下列有关物质的性质与用途具有对应关系的是
A.稀硫酸有酸性,可用于除去铁锈
B.Al2O3具有两性,可用于电解冶炼铝
C.SO2能使酸性高锰酸钾溶液褪色,可用于漂白有色物质
D.甲醛溶液能使蛋白质发生变性,可用于动物标本的防腐
【答案】AD
【解析】
A.铁锈的主要成分为氧化铁,稀硫酸能和氧化铁反应生成可溶性的硫酸铁和水,所以可以除铁锈,该反应中体现了稀硫酸的酸性,A符合题意;
B.氧化铝在熔融状态下能导电且铝比较活泼,工业上用电解氧化铝的方法冶炼铝,用电解法冶炼铝与氧化铝的两性无关,B不符题意;
C.SO2能使酸性高锰酸钾溶液褪色是因为SO2具有还原性,SO2用于漂白有色物质是利用其漂白性,性质与用途不具有对应关系,C不符题意;
D.甲醛有毒性,可使蛋白质变性,具有杀菌、防腐的用途,35%![]() 40%的甲醛水溶液叫福尔马林,可用于动物标本的防腐,性质与用途具有对应关系,D符合题意。
40%的甲醛水溶液叫福尔马林,可用于动物标本的防腐,性质与用途具有对应关系,D符合题意。
答案选AD。

【题目】某地菱锰矿的主要成分为MnCO3,还含有少量的FeCO3、CaCO3、Al2O3等杂质。工业上以菱锰矿为原料制备高纯度碳酸锰的流程如图所示:
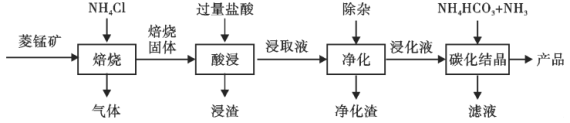
已知:MnCO3+2NH4Cl=MnCl2+CO2↑+2NH3↑+H2O.
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 |
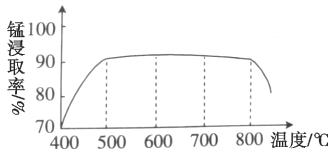
(1)焙烧时温度对锰浸取率的影响如图。焙烧时适宜的温度为___________左右;800℃以上锰的浸取率偏低,可能的原因是___________。
(2)净化包含三步:①加入少量MnO2,添加少量MnO2的作用是____________。发生反应的离子方程式为___________。
②加氨水调pH,溶液的pH范围应调节为___________~8.1之间。生成的沉淀主要是___________。
③加入MnF2,沉淀除去Ca2+,若溶液酸度过高,Ca2+沉淀不完全,原因是___________。
(3)碳化结晶中生成MnCO3的离子方程式为____________。
【题目】某实验小组用0.55mol/LNaOH溶液和0.50mol/LHCl溶液进行中和热的测定。测定中和热的实验装置如图所示。

(1)从实验装置上看,图中缺少的一种玻璃仪器__________。
(2)使用补全仪器后的装置进行实验,取50mL0.50mol/LHCl溶液与50mL0.55mol/LNaOH溶液在小烧杯中进行中和反应,实验数据如表。
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值(t2-t1)/℃ | ||
HCl | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | ______℃ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
①请填写表中的空白:温度差平均值__________℃
②上述实验数值结果比中和热57.3kJ/mol偏小,产生的原因可能是______。(填字母)
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定HCl溶液的温度
(3)实验中若用60mL0.25mol/LH2SO4溶液跟50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量______(填“相等”、“不相等”),所求中和热______(填“相等”、“不相等”),若用50mL0.50mol/L醋酸代替HCl溶液进行上述实验,测得反应前后温度的变化值会______(填“偏大”、“偏小”、“不受影响”)