题目内容
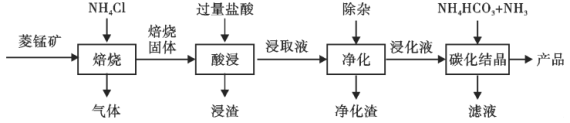
【题目】某地菱锰矿的主要成分为MnCO3,还含有少量的FeCO3、CaCO3、Al2O3等杂质。工业上以菱锰矿为原料制备高纯度碳酸锰的流程如图所示:
已知:MnCO3+2NH4Cl=MnCl2+CO2↑+2NH3↑+H2O.
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 |
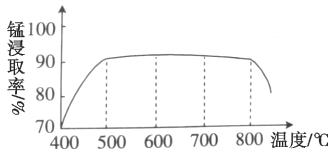
(1)焙烧时温度对锰浸取率的影响如图。焙烧时适宜的温度为___________左右;800℃以上锰的浸取率偏低,可能的原因是___________。
(2)净化包含三步:①加入少量MnO2,添加少量MnO2的作用是____________。发生反应的离子方程式为___________。
②加氨水调pH,溶液的pH范围应调节为___________~8.1之间。生成的沉淀主要是___________。
③加入MnF2,沉淀除去Ca2+,若溶液酸度过高,Ca2+沉淀不完全,原因是___________。
(3)碳化结晶中生成MnCO3的离子方程式为____________。
【答案】500℃ 温度过高,NH4Cl分解导致与MnCO3的反应不彻底(或MnCO3分解发生其他副反应;或MnCl2挥发导致Mn损失;或高温下锰被氧化成高价态造成浸取率低;或高温使固体烧结,固体表面积减小等) 将Fe2+氧化为Fe3+ MnO2+2Fe2++4H+===Mn2++2Fe3++2H2O 4.7 Fe(OH)3、Al(OH)3 F- 与H+ 结合形成弱电解质HF,CaF2(s)![]() Ca2+(aq)+F—(aq)平衡向右移动 )Mn2++HCO3-+NH3===MnCO3↓+NH4+
Ca2+(aq)+F—(aq)平衡向右移动 )Mn2++HCO3-+NH3===MnCO3↓+NH4+
【解析】
(1)由图示得到,500 ℃时,锰的浸取率已经很大;温度很高时,氯化铵受热分解、MnCO3分解发生其他副反应等;
(2)①加入二氧化锰的目的是为了将Fe2+氧化为Fe3+;
②加氨水调溶液pH的目的是使溶液中Fe3+和Al3+转化为Fe(OH)3沉淀和Al(OH)3沉淀除去;
③若溶液酸度过高,F- 与H+ 结合形成弱酸HF,使CaF2溶解平衡向右移动;
(3)碳化结晶是氯化锰溶液与碳酸氢铵和氨水应得到碳酸锰沉淀。
(1)由图示得到,500 ℃时,锰的浸取率已经很大,所以选取500℃即可,没有必要选择更高的温度,因为温度越高,能耗越大;温度很高时,浸取率下降,有可能是高温下氯化铵分解使反应的量减少;或生成的氯化锰转化为气体离开体系;或高温下发生副反应,锰转化为其他化合物;或高温使固体烧结,固体表面积减小等,故答案为:500℃;温度过高,NH4Cl分解导致与MnCO3的反应不彻底(或MnCO3分解发生其他副反应;或MnCl2挥发导致Mn损失;或高温下锰被氧化成高价态造成浸取率低;或高温使固体烧结,固体表面积减小等);
(2)①加入二氧化锰的目的是为了将Fe2+氧化为Fe3+,反应的化学方程式为MnO2+2Fe2++4H+===Mn2++2Fe3++2H2O,故答案为:MnO2+2Fe2++4H+===Mn2++2Fe3++2H2O;
②加氨水调溶液pH的目的是使溶液中Fe3+和Al3+转化为Fe(OH)3沉淀和Al(OH)3沉淀除去,由题给表格数据可知,溶液的pH范围调节在4.7~8.1之间时,Fe3+和Al3+完全沉淀,而Mn2+不沉淀,故答案为:4.7;
③加入MnF2目的是沉淀除去Ca2+,CaF2在溶液中存在溶解平衡CaF2(s)![]() Ca2+(aq)+F—(aq),若溶液酸度过高,F- 与H+ 结合形成弱酸HF,F—浓度减小,溶解平衡向右移动,使Ca2+沉淀不完全,故答案为:F- 与H+ 结合形成弱电解质HF,CaF2(s)
Ca2+(aq)+F—(aq),若溶液酸度过高,F- 与H+ 结合形成弱酸HF,F—浓度减小,溶解平衡向右移动,使Ca2+沉淀不完全,故答案为:F- 与H+ 结合形成弱电解质HF,CaF2(s)![]() Ca2+(aq)+F—(aq)平衡向右移动;
Ca2+(aq)+F—(aq)平衡向右移动;
(3)碳化结晶是向氯化锰溶液中加入碳酸氢铵和氨水,反应得到碳酸锰沉淀,反应的化学方程式为Mn2++HCO3-+NH3===MnCO3↓+NH4+,故答案为:Mn2++HCO3-+NH3===MnCO3↓+NH4+。

 阅读快车系列答案
阅读快车系列答案【题目】已知K2Cr2O7溶液中存在平衡:Cr2O72-+H2O ![]() 2CrO42-+2H+。K2Cr2O7为橙色,K 2CrO4为黄色。为探究浓度对化学平衡的影响,某兴趣小组设计了如下实验方案。
2CrO42-+2H+。K2Cr2O7为橙色,K 2CrO4为黄色。为探究浓度对化学平衡的影响,某兴趣小组设计了如下实验方案。
| 序号 | 试剂X |
ⅰ | 1 mL1mol·L-1 K2Cr2O7 溶液 | |
ⅱ | 1mL1 mol·L-1 K2CrO4溶液 | |
ⅲ | 5~15滴浓硫酸 | |
ⅳ | 5~15滴浓盐酸 | |
ⅴ | 5~15滴6 mol·L-1 NaOH溶液 |
Ⅰ.方案讨论
(1)ⅰ~ⅴ中依据减少生成物浓度可导致平衡移动的原理设计的是______(填序号)。
(2)已知BaCrO4为黄色沉淀。某同学认为试剂X还可设计为Ba(NO3)2溶液,加入该试剂后,溶液颜色将_____。(填“变深”、“变浅”或“不变”)。
Ⅱ.实验分析
序号 | 试剂X | 预期现象 | 实际现象 |
ⅰ | 1 mL1 mol·L-1 K2Cr2O7 溶液 | 溶液变黄 | 溶液橙色加深 |
ⅱ | 1mL1 mol·L-1 K2CrO4溶液 | 溶液橙色加深 | 溶液颜色变浅 |
ⅲ | 5~15滴浓硫酸 | 溶液橙色加深 | 溶液橙色加深 |
ⅳ | 5~15滴浓盐酸 | 溶液橙色加深 | 无明显现象 |
ⅴ | 5~15滴6mol·L-1NaOH溶液 | 溶液变黄 | 溶液变黄 |
(1)实验ⅰ没有观察到预期现象的原因是____________,实验ⅱ的原因与其相似。
(2)通过实验ⅲ和ⅴ得出的结论为___________ 。
(3)实验ⅳ无明显现象,可能的原因是____________。
(4)某同学查阅资料发现:K2Cr2O7溶液与浓盐酸可发生氧化还原反应。但实验ⅳ中没有观察到明显现象,小组同学设计了两个实验,验证了该反应的发生。
① 方案一:取5 mL浓盐酸,向其中加入15滴0.1mol·L-1 K2Cr2O7溶液,一段时间后,溶液变为绿色(CrCl3水溶液呈绿色),有黄绿色气体生成。写出该变化的化学方程式__________。
② 请你设计方案二:_______________。
【题目】有机物A仅含有C、H、O三种元素,可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
限选试剂:蒸馏水、2 mol·L-1盐酸溶液、2 mol·L-1NaOH溶液、浓硫酸、NaHCO3粉末、金属Na、无水乙醇
实验步骤 | 实验结论 |
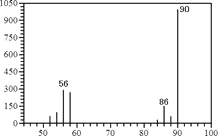
(1)A的质谱图如下: | (1)证明A的相对分子质量为:__________。 |
(2)将此9.0 g A在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现分别增重5.4 g和13.2 g。 | (2)证明A的分子式为: ________________。 |
(3)另取两份9.0 g A分置于不同的试管中。往其中一份A中加入足量的NaHCO3粉末充分反应,生成_______ L CO2(标准状况)。 往另一份A中加入足量的金属钠充分反应,生成________________________ L H2(标准状况)。 | (3)证明A的分子中含有一个羧基和一个羟基。 |
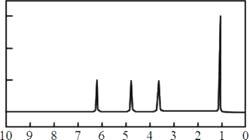
(4)A的核磁共振氢谱如下图: | (4)A的结构简式为: __________________。 |