题目内容
【题目】(1)CH3COOH是最常见的有机弱酸。
①CH3COOH的电离方程式为_____________。
②CH3COONa溶液呈碱性,原因是__________(填“CH3COO-”或“Na+”)水解引起的。
③ 在CH3COONa溶液中,c(Na+)_______c(CH3COO-)、(填“>”“=”或“<”)
(2)已知:反应C(s)+H2O(g)![]() CO(g)+H2(g)的△H=131.3kJ/mol
CO(g)+H2(g)的△H=131.3kJ/mol
① 该反应是反应__________(填“吸热”或“放热”)。
② 若反应消耗24gC(s),则反应的热效应为__________。
(3)在一定温度下,将CO(g)和H2O(g)各0.16 mol 通入容积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
t/min | 2 | 4 | 7 | 9 |
n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
① 2 min 内,vCO=__________。
② 该温度下,此反应的平衡常数表达式K=_________。
③ 其他条件不变,再充入0.1molCO和0.1molH2O(g),达到平衡时CO 的休积分数_____(填“增大”、“减小”或“不变”)。
(4)下图为直流电源电解CuSO4溶液的装置,C1和C2都为石墨电极,请回答下列问题:
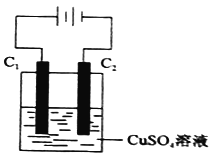
① C1作_________(填“阳极”或”阴极”)。
② C2极电极反应式为____________。
【答案】 CH3COOH![]() CH3COO-+H+ CH3COO- > 吸热 吸热262.6kJ 0.01mol/(L·min)
CH3COO-+H+ CH3COO- > 吸热 吸热262.6kJ 0.01mol/(L·min) ![]() 不变 阳极 【答题空10】Cu2++2e-=Cu
不变 阳极 【答题空10】Cu2++2e-=Cu
【解析】(1)CH3COOH是最常见的有机弱酸。
①CH3COOH是弱酸,电离方程式为CH3COOH![]() CH3COO-+H+;②CH3COONa溶液呈碱性,原因是CH3COO- 水解引起的,CH3COO―+H2O
CH3COO-+H+;②CH3COONa溶液呈碱性,原因是CH3COO- 水解引起的,CH3COO―+H2O ![]() CH3COOH+OH― ;③ 在CH3COONa溶液中,CH3COO- 水解,Na+ 不水解,故c(Na+)> c(CH3COO-);(2)①反应的△H=131.3kJ/mol 为正表示吸热反应;② 若反应消耗24gC(s),则反应的热效应为吸收
CH3COOH+OH― ;③ 在CH3COONa溶液中,CH3COO- 水解,Na+ 不水解,故c(Na+)> c(CH3COO-);(2)①反应的△H=131.3kJ/mol 为正表示吸热反应;② 若反应消耗24gC(s),则反应的热效应为吸收![]() ;(3)① 2 min 内,vCO=v(H2O)=
;(3)① 2 min 内,vCO=v(H2O)=![]() ;② 该温度下,此反应的平衡常数表达式K=
;② 该温度下,此反应的平衡常数表达式K=![]() ;③CO(g)+H2O(g)
;③CO(g)+H2O(g) ![]() CO2(g)+H2(g)是体积不变的反应,按反应物比例增加投料,相当加压平衡不移动,达到平衡时CO 的休积分数不变。(4) C1与外电源的正极相连,作阳极,电解硫酸铜,阳极上电极反应:4OH--4e-=2H2O+O2↑,生成1mol氧气消耗4mol氢氧根离子,阴极 C2极电极反应式为:Cu2++2e-=Cu。
CO2(g)+H2(g)是体积不变的反应,按反应物比例增加投料,相当加压平衡不移动,达到平衡时CO 的休积分数不变。(4) C1与外电源的正极相连,作阳极,电解硫酸铜,阳极上电极反应:4OH--4e-=2H2O+O2↑,生成1mol氧气消耗4mol氢氧根离子,阴极 C2极电极反应式为:Cu2++2e-=Cu。