题目内容
【题目】下表是元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答下列问题。
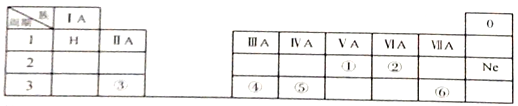
(1)①的原子结构示意图为_________。
(2)③和④两种元素金属性强弱关系是:③______(填“>”或“<”)④
(3)③和⑥两种元素形成的化合物中含有的化学键为_______(填“离子键”或“共价键”) 。
(4)④和⑥组成的化合物的水溶液与AgNO3溶液反应的离子方程式为____________。
【答案】 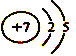 > 离子键 Ag++Cl-=AgCl↓
> 离子键 Ag++Cl-=AgCl↓
【解析】由元素在周期表中位置,可知①为N、②为O、③为Mg、④为Al、⑤为Si、⑥为Cl。(1)①的原子结构示意图为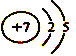 ;(2)同周期随原子序数增大,原子半径减小,金属性减弱,故金属性减弱Mg>Al,故答案为:>;(3)③位于第三周期第ⅡA族,是Mg元素,⑥位于第三周期第ⅦA族,是Cl元素,形成的化合物是离子化合物MgCl2,两种元素形成的化合物中含有的化学键为离子键;(4)④和⑥组成的化合物的水溶液为AlCl3,与AgNO3溶液反应的离子方程式为Ag++Cl-=AgCl↓。
;(2)同周期随原子序数增大,原子半径减小,金属性减弱,故金属性减弱Mg>Al,故答案为:>;(3)③位于第三周期第ⅡA族,是Mg元素,⑥位于第三周期第ⅦA族,是Cl元素,形成的化合物是离子化合物MgCl2,两种元素形成的化合物中含有的化学键为离子键;(4)④和⑥组成的化合物的水溶液为AlCl3,与AgNO3溶液反应的离子方程式为Ag++Cl-=AgCl↓。

 应用题作业本系列答案
应用题作业本系列答案【题目】A、B、C、D、E、 F、G是周期表中短周期的七种元素,有关性质或结构信息如下表:
元素 | 有关性质或结构信息 |
A | 地壳中含量最多的元素 |
B | B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的 |
C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
D | D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
E | E与D同周期,且在该周期中原子半径最小 |
F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
G | G是形成化合物种类最多的元素 |
(1) B元素符号为____,A与C以原子个数比为1:1形成的化合物的电子式为___,用电子式表示C与E形成化合物的过程____, D形成的简单离子的结构示意图为____。
(2) F的氢化物是由____(极性或非极性)键形成的分子,写出实验室制备该氢化物的化学方程式____。
(3) 非金属性D____E(填大于或小于),请从原子结构的角度解释原因:__。
【题目】(1)CH3COOH是最常见的有机弱酸。
①CH3COOH的电离方程式为_____________。
②CH3COONa溶液呈碱性,原因是__________(填“CH3COO-”或“Na+”)水解引起的。
③ 在CH3COONa溶液中,c(Na+)_______c(CH3COO-)、(填“>”“=”或“<”)
(2)已知:反应C(s)+H2O(g)![]() CO(g)+H2(g)的△H=131.3kJ/mol
CO(g)+H2(g)的△H=131.3kJ/mol
① 该反应是反应__________(填“吸热”或“放热”)。
② 若反应消耗24gC(s),则反应的热效应为__________。
(3)在一定温度下,将CO(g)和H2O(g)各0.16 mol 通入容积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
t/min | 2 | 4 | 7 | 9 |
n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
① 2 min 内,vCO=__________。
② 该温度下,此反应的平衡常数表达式K=_________。
③ 其他条件不变,再充入0.1molCO和0.1molH2O(g),达到平衡时CO 的休积分数_____(填“增大”、“减小”或“不变”)。
(4)下图为直流电源电解CuSO4溶液的装置,C1和C2都为石墨电极,请回答下列问题:
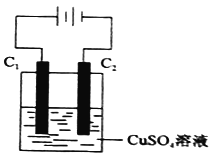
① C1作_________(填“阳极”或”阴极”)。
② C2极电极反应式为____________。
