题目内容
7.实验室用NaOH 固体配制1.0mol/L的NaOH溶液500mL,回答下列问题(1)配制溶液所需仪器为:500mL容量瓶、托盘天平、药匙、烧怀、玻璃棒、胶头滴管,称取的NaOH的质量为20.0g
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)B、C、A、F、E、D;
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.将NaOH固体置于烧杯中用天平准确称取质量,再在烧杯中加入少量水(约50mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(3)操作A中,将洗涤液都移入容量瓶,其目的是保证溶质全部转入容量瓶
(4)在配制该物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏低ADEF
A.称量固体NaOH时,有潮解现象
B.定容时俯视容量瓶的刻度线观察液面
C.称量时误用“左码右物”
D.未洗涤烧杯以及玻璃棒
E.定容时仰视容量瓶的刻度线观察液面
F.定容后,加盖倒转摇匀后,发现液面低于刻度线,又加水至刻度
G.容量瓶中原有少量蒸馏水.
分析 (1)根据操作步骤选取实验仪器;根据m=nM=cVM计算需要氢氧化钠的质量;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来对操作顺序进行排序;
(3)如果不将洗涤液均转移至容量瓶,会导致溶质的损失;
(4)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析.
解答 解:(1)配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水),冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2~3次,将洗涤液移入容量瓶,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加;所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管;
配制500mL1mol/L NaOH溶液需要氢氧化钠的质量为1mol/L×0.5L×40g/mol=20.0g.
故答案为:500mL容量瓶;20.0g;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序为B、C、A、F、E、D,故答案为:B、C、A、F、E、D;
(3)如果不将洗涤液均转移至容量瓶,会导致溶质的损失,故目的是保证所有的溶质均转移至容量瓶中,故答案为:保证溶质全部转入容量瓶;
(4)A.称量固体NaOH时,有潮解现象,会导致所称量的固体中氢氧化钠的真实质量偏小,则浓度偏低,故A选;
B.定容时俯视容量瓶的刻度线观察液面,则溶液体积偏小,浓度偏高,故B不选;
C.由于所称量的氢氧化钠的质量为20.0g,不用游码,故称量时误用“左码右物”,对所称量的固体的质量无影响,即对溶液的浓度无影响,故B不选;
D.未洗涤烧杯以及玻璃棒,会导致溶质损失,则浓度偏低,故D选;
E.定容时仰视容量瓶的刻度线观察液面,则溶液的体积偏大,则浓度偏低,故E选;
F.定容后,加盖倒转摇匀后,发现液面低于刻度线是正常的,又加水至刻度,则浓度偏低,故F选;
G.若容量瓶未干燥即用来配制溶液,对溶液浓度无影响,因为只要定容时正确,至于水是原来就有的还是后来加入的,对浓度无影响,故G不选;
故答案为:ADEF.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.

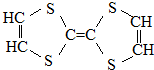
| A. | 它属于烃的衍生物 | B. | 所有的碳杂化方式相同 | ||
| C. | 属于高分子化合物 | D. | 它可以与氢气加成 |
| A. | 雷雨时,可增加土壤中硝酸盐类氮肥的含量 | |
| B. | 许多领域中用液氮制得低温环境 | |
| C. | 造成光化学烟雾的罪魁祸首是SO2 | |
| D. | 正常雨水因溶有CO2,其pH约为5.6,而酸雨的pH小于5.6 |
| A. | N2 | B. | HCl | C. | NaCl | D. | KOH |
| 物质(括号中为杂志) | 所加试剂 | 操作方法 |
| 酒精(水) | 新制生石灰 | 蒸馏 |
苯甲酸(沙子) | / | 过滤 |
| 甲烷(乙烯) | 溴水(溴的四氯化碳溶液) | 洗气 |
| 溴苯(溴) | 氢氧化钠溶液 | 分液 |
| A. | 电解池的阳极发生氧化反应,阴极上发生还原反应 | |
| B. | 不能自发进行的氧化还原反应可通过电解的原理实现 | |
| C. | 电镀时,电镀池里的阳极材料发生氧化反应 | |
| D. | 电解饱和食盐水时,阳极得到,NaOH溶液和氢气 |