题目内容
17.用于制造隐形飞机物质具有吸收微波的功能,其主要成分的结构如图,说法不正确的是( )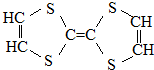
| A. | 它属于烃的衍生物 | B. | 所有的碳杂化方式相同 | ||
| C. | 属于高分子化合物 | D. | 它可以与氢气加成 |
分析 有机物含有S等元素,属于烃的衍生物,含有碳碳双键,可发生加成、加聚和氧化反应,结合高分子化合物的定义解答该题.
解答 解:A.有机物含有S等元素,属于烃的衍生物,故A正确;
B.C原子都形成C=C键,都为sp2杂化,故B正确;
C.高分子化合物的相对分子质量在10000以上,该有机物不是高分子化合物,故C错误;
D.含有碳碳双键,可与氢气发生加成反应,故D正确.
故选C.
点评 本题考查有机物的结构和性质,题目难度不大,本题注意把握有机物的官能团的性质,注意烃、烃的衍生物的概念,侧重烯烃性质的考查.

练习册系列答案
相关题目
4.下列说法中,不正确的是( )
| A. | 氢氧化铁胶体中分散质微粒直径为1~100nm | |
| B. | 可用丁达尔现象判断胶体的制备是否成功 | |
| C. | 溶液一定是均一、稳定的混合物 | |
| D. | 长期放置后不会分层的液体,就是溶液 |
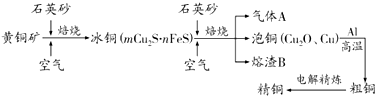
12.用含有A1203、SiO2和少量FeO•xFe2O3的铝灰制备A12(SO4)3•18H2O.,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品.
(1)H2S04溶解A12O3的离子方程式是Al2O3+6H+=2Al3++3H2O.
(2)请将KMnO4氧化Fe2+的离子方程式补充完整:
□MnO4-+□Fe2++□8H+=□Mn2++□Fe3++□4H2O
(3)生成各种氢氧化物沉淀的pH如下表(金属离子的起始浓度为0.1mol•L-1)
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀.
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnS04的目的是除去过量的MnO4-.
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品.
(1)H2S04溶解A12O3的离子方程式是Al2O3+6H+=2Al3++3H2O.
(2)请将KMnO4氧化Fe2+的离子方程式补充完整:
□MnO4-+□Fe2++□8H+=□Mn2++□Fe3++□4H2O
(3)生成各种氢氧化物沉淀的pH如下表(金属离子的起始浓度为0.1mol•L-1)
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnS04的目的是除去过量的MnO4-.
2. 许多物质在通常条件下是以晶体的形式存在,而一种晶体又可视作若干相同的基本结构单元构成,这些基本结构单元在结构化学中被称作晶胞.已知某化合物是由钙、钛、氧三种元素组成的晶体,其晶胞结构如图所示,则该物质的化学式为( )
许多物质在通常条件下是以晶体的形式存在,而一种晶体又可视作若干相同的基本结构单元构成,这些基本结构单元在结构化学中被称作晶胞.已知某化合物是由钙、钛、氧三种元素组成的晶体,其晶胞结构如图所示,则该物质的化学式为( )
 许多物质在通常条件下是以晶体的形式存在,而一种晶体又可视作若干相同的基本结构单元构成,这些基本结构单元在结构化学中被称作晶胞.已知某化合物是由钙、钛、氧三种元素组成的晶体,其晶胞结构如图所示,则该物质的化学式为( )
许多物质在通常条件下是以晶体的形式存在,而一种晶体又可视作若干相同的基本结构单元构成,这些基本结构单元在结构化学中被称作晶胞.已知某化合物是由钙、钛、氧三种元素组成的晶体,其晶胞结构如图所示,则该物质的化学式为( )| A. | Ca4TiO6 | B. | Ca4TiO3 | C. | Ca8TiO12 | D. | CaTiO3 |
6.下列有关物质分类正确的组合是( )
| 酸 | 碱 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | 盐酸 | 纯碱 | 烧碱 | 氧化铝 | 二氧化碳 |
| B | 硫酸 | 烧碱 | 食盐 | 氧化钙 | 一氧化碳 |
| C | 醋酸 | 苛性碱 | 小苏打 | 一氧化碳 | 二氧化硫 |
| D | 硫酸 | 苛性钾 | 苏打 | 氧化铜 | 三氧化硫 |
| A. | A | B. | B | C. | C | D. | D |
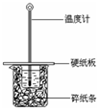 某实验小组用0.55mol/L NaOH溶液和0.50mol/L盐酸反应来测定中和热,实验装置如图所示.
某实验小组用0.55mol/L NaOH溶液和0.50mol/L盐酸反应来测定中和热,实验装置如图所示.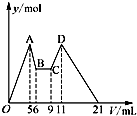 有氯化铝和氯化镁的混合溶液,向其中滴加a mL 3mol•L-1 NaOH溶液之后,改成滴加cmol/L HCl溶液,所得沉淀的物质的量y(mol)与试剂总体积V(mL)间的关系如图所示.请回答下列问题:
有氯化铝和氯化镁的混合溶液,向其中滴加a mL 3mol•L-1 NaOH溶液之后,改成滴加cmol/L HCl溶液,所得沉淀的物质的量y(mol)与试剂总体积V(mL)间的关系如图所示.请回答下列问题: