题目内容
19.下列叙述正确的是( )| A. | 直径介于1nm~100nm之间的微粒称为胶体 | |
| B. | 电泳现象可证明胶体属于电解质溶液 | |
| C. | 胶体粒子很小,可以透过半透膜 | |
| D. | 利用丁达尔效应可以区别溶液与胶体 |
分析 A.当分散剂是水或其它溶液时,根据分散质粒子直径大小来分类,把分散系划分为:溶液(小于1nm)、胶体(1nm~100nm)、浊液(大于100nm);
B.胶体属于混合物,电解质是化合物,电泳能证明胶体属电解质溶液;
C.根据胶体粒子大小分析,胶体粒子不可以透过半透膜;
D.胶体具有丁达尔效应,是胶体特有的性质,溶液不具有丁达尔效应.
解答 解:A.直径介于1nm~100nm之间的微粒可能为纯净物,当分散剂是水或其它溶液时,分散质粒子直径大小在1nm~100nm之间的是胶体,故A错误;
B.胶体具有吸附性,胶体的胶粒吸附胶体中带电荷的离子带电,如氢氧化铁胶体的胶粒吸附三价铁离子,带正电荷,通电后,氢氧化铁胶体的胶粒向阴极移动,产生电泳现象,电解质是指:在水溶液中或熔融状态下能够导电的化合物,胶体属于混合物,所以电泳现象能证明胶体属电解质溶液,故B错误;
C.胶体粒子直径大于半透膜孔隙,不可以透过半透膜,故C错误;
D.光线透过胶体时,胶体中可发生丁达尔效应,丁达尔效应是胶体特有的性质,溶液不具有丁达尔效应,利用丁达尔效应可以区别溶液与胶体,故D正确;
故选D.
点评 本题考查了胶体粒子的大小及胶体的性质,侧重于基础知识的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.一定温度下,反应N2(g)+3H2(g)?2NH3(g)达到化学平衡状态的标志是( )
| A. | N2、H2和NH3的质量分数不再改变 | |
| B. | c(N2):c(H2):c(NH3)=1:3:2 | |
| C. | 单位时间里每增加1molN2,同时减少2mol NH3 | |
| D. | 单位时间里每增加1molN2,同时增加3molH2 |
10.知反应:A(g)+B(g)?C(g)+D(g)的能量变化如图所示,下列说法正确的是( )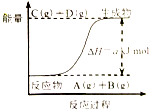

| A. | 若此反应过程中有电子转移,可设计成原电池 | |
| B. | 当A、B、C、D的浓度相同时,反应处于平衡状态 | |
| C. | 当A的消耗速率与C的消耗速率相同时处于平衡状态 | |
| D. | 该反应只有在加热条件下才能进行 |
14.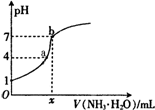 向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示.下列判断正确的是( )
向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示.下列判断正确的是( )
 向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示.下列判断正确的是( )
向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示.下列判断正确的是( )| A. | x=20 | B. | 稀H2SO4的浓度为0.10mol/L | ||
| C. | b点有:2c(NH4+)=c(SO42-)>c(H+)=c(OH-) | D. | a点有:c(NH4+)<2c(SO42-) |
4.乳酸的结构简式是CH3-CH(OH)-COOH,下列有关乳酸的说法中正确的是( )
| A. | 乳酸中不含羟基 | |
| B. | 乳酸不能发生消去反应 | |
| C. | 乳酸与足量钠反应时物质的量之比为1:1 | |
| D. | 乳酸与足量NaOH溶液反应时物质的量之比为1:1 |
8.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1molSiO2含有2NA个Si-O键 | |
| B. | 1molNa2O2固体中含离子总数为3NA. | |
| C. | 标准状况下,22.4 L SO3所含分子数为NA. | |
| D. | 1L0.5mol/L的MgCl2溶液中,含有Mg2+个数为0.5NA. |
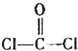 的空间结构为平面三角形.
的空间结构为平面三角形.