��Ŀ����
����Ŀ����NaClΪ��Ҫ�ɷֵ���ѩ���ḯʴ����������ȸ����豸��ij�о�С��̽��NaCl��Һ�Ը�����ʴ��Ӱ�졣
��1������ֽ��3.5%��NaCl��Һ��ʪ��Ϳ�����ۡ�̼�۵Ļ������ڱ������ϡ�����ֽ�ϼӼ��μ����Լ����ٻ�������NaCl��Һ��û����ֽ������������ʾ��

��ʵ����������˵�����õ��ӵ�������_______________________________��
��̼�۵�������___________________________________________________��
��Ϊ��˵��NaCl�����ã���Ҫ����Ķ���ʵ����_____________________��
��2������ͼʾװ�õ��ձ�a��b�и�����30mL 3.5%��NaCl��Һ���պ�K��ָ��δ����ƫת�������ձ�a��ָ������ƫת��

��ȡa��b����Һ�������μ�K3[Fe(CN)6]��Һ��a�г�����ɫ������b���ޱ仯��b����Ƭ��________����
�ڼ��Ⱥ�ָ�뷢��ƫת��ԭ�������_____________________��
��3���ã�2����ͼʾװ��̽����ͬŨ��NaCl��Һ�Ը�����ʴ��Ӱ�죬���ձ�a��b�и�����30mL��ͬ����������NaCl��Һ��ʵ���¼���±���ʾ��
ʵ�� | a | b | ָ��ƫת���� |
I | 0.1% | 0.01% | ���� |
II | 0.1% | 3.5% | ���� |
�� | 3.5% | ������Һ | ���� |
�����У�b�е缫�����ĵ缫��Ӧʽ��_______________________________��
�����У����ڱ���NaCl��Һ�в��ױ���ʴ���������Ͽ�֪���ڱ���NaCl��Һ��O2Ũ�Ƚϵͣ��������ױ���ʴ�����ʵ��֤����_______________________________��
��4����������ʵ�飬�Ը�����ʴ��Ӱ���������_______________________________��
���𰸡�O2 �������ԭ��أ���ԭ��ص����� ��ˮ����NaCl��Һ��������ʵ�� �� �¶����ߣ�Fe��ԭ����ǿ����Ӧ���ʼӿ� Fe��2e-=Fe2+ ��ȡ�����ձ����ֱ������м�����Ƭ��һ�����ı���NaCl��Һ���ٷֱ�μӼ���K3Fe(CN)6��Һ��Ȼ��������һ���ձ���ͨ��O2���۲����� �¶ȡ�NaCl��Һ��Ũ�ȡ�O2��Ũ��
��������
��1������̼���Ȼ�����ҺΪ������γ�ԭ��أ�����������ʴ�������������ӣ���Һ�Լ��ԣ�������̪��죻
��2����K3[Fe(CN)6]��Һ����������ӷ�Ӧ������ɫ������
���¶����ߣ�Fe��ԭ����ǿ����Ӧ���ʼӿ죻
��3�������ݲ�ͬŨ���£�������ָ��ƫת�����жϵ缫����д�缫��Ӧʽ��
��Ҫ֤���ڱ���NaCl��Һ��O2Ũ�Ƚϵͣ��������ױ���ʴ��������ƶԱ����飬һ��ʵ����ͨ����������һ��ʵ���в�ͨ���������۲����ĸ�ʴ�����
��4����������ʵ���ܽ���ɽ��
��1��������̼���Ȼ�����ҺΪ������γ�ԭ��أ���̪���˵���������������ӣ�����������ʴ���ʵõ��ӵ�������O2��
������̼���Ȼ�����ҺΪ������γ�ԭ�磬����ԭ��ظ�����̼��������
��Ϊ��˵��NaCl�����ã���Ҫ����Ķ���ʵ���ǣ���ˮ������ʣ������Ȼ��ƽ�������ʵ�飻
��2����K3[Fe(CN)6]��Һ����������ӷ�Ӧ������ɫ��������ȡa��b����Һ�������μ�K3[Fe(CN)6]��Һ��a�г�����ɫ������˵��a�����ɶ��������ӣ�b���ޱ仯��b��û�ж������������ɣ�����a��������b��������
�����Ⱥ�ָ�뷢��ƫת��ԭ������ǣ��¶����ߣ�Fe��ԭ����ǿ����Ӧ���ʼӿ죻
��3��������ͼ�����������ݼ�ָ������ƫת�����֪��b��Ϊ������ʧȥ���ӷ���������Ӧ���缫��Ӧʽ��Fe��2e-=Fe2+��
��Ҫ֤������Ũ�ȶԽ�����ʴ���ʵ�Ӱ�죬������ƶԱ�ʵ�飬���£���ȡ�����ձ����ֱ������м�����Ƭ��һ�����ı���NaCl��Һ���ٷֱ�μӼ���K3Fe(CN)6��Һ��Ȼ��������һ���ձ���ͨ��O2���۲�����
��4��ͨ������ʵ���֪���Ը�����ʴ��Ӱ������������¶ȡ�NaCl��Һ��Ũ�ȡ�O2��Ũ�ȡ�

 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�����Ŀ��Ŀǰ����β���е�NO���������¼��ַ�����
��1���������������ϰ�װ��ת������NO��CO�����Ϊ����β���ijɷ֣������������ڴ�ת�����з�����Ӧ��2CO(g)��2NO(g)![]() N2(g)��2CO2(g) ��H ��
N2(g)��2CO2(g) ��H ��
����֪��N2(g)+O2(g)=2NO(g)��H1����180.5kJ��mol��1��C(s)+O2(g)=CO2(g) ��H2����393.5 kJ��mol��1��2C(s)+O2(g)=2CO(g)��H3����221kJ��mol��1������H=______��
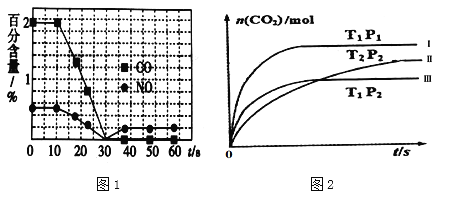
��һ����ȤС���ij����������ʱ��β��������������CO��NO�ٷֺ�����ʱ��仯��ͼ1��ʾ��ǰ0��10s �Σ�CO��NO�ٷֺ���û���Ա仯��ԭ����_____________________��ͬʱ��С���ڹ̶��ݻ�Ϊ2L���ܱ�������ͨ��NO��CO��2mol���з�Ӧ��n(CO2)���¶ȣ�T����ѹǿ��P����ʱ�䣨t���ı仯������ͼ2��ʾ��ͼ�е�����������������Ӧ��Ӧ�ӿ�ʼ��ƽ��ʱ��CO2��ʾ��ƽ����Ӧ���ʷֱ�Ϊv(��)��v��������v�������������ߴ�С��ϵΪ______________��
��2������̿Ҳ�����ڴ�������β���е�NO����1L�����ܱ������м���0.1000molNO��2.030mol�������̿������CO2��N2�������壬�ڲ�ͬ�¶��²��ƽ����ϵ�и����ʵ����ʵ����Լ�������ѹǿ���±���
����̿/mol | NO/mol | CO2/mol | N2/mol | P/MPa | |
200�� | 2.000 | 0.0400 | 0.0300 | 0.0300 | 3.93 |
X | 2.005 | 0.0500 | 0.0250 | 0.0250 | 4.56 |
�����з�����Ӧ�Ļ�ѧ����ʽΪC(s) +2NO(g) CO2(g) +N2(g)�������ϱ����ݣ����ж�X_____200������������������������=����գ������㷴Ӧ��ϵ��200��ʱ��ƽ�ⳣ��Kp=_____����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�������������
��3���ü�ӵ绯ѧ����ȥNO�Ĺ��̣���ͼ��ʾ����֪���ص�����������Һ��pH��4~7֮�䣬B��Ϊ_________(��������������������)��д��A���ĵ缫��Ӧʽ��____________��