题目内容
9.元素周期表可以划分为5个区,下列有关说法正确的是( )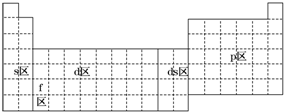
| A. | s区全部是金属元素 | |
| B. | p区全部是非金属元素 | |
| C. | d区内元素原子的价电子排布必为(n-1)d1~10ns2 | |
| D. | 除ds区外,以最后填入电子的轨道能级符号作为区的符号 |
分析 A、s区元素除氢元素都是金属元素;
B、除氢外所有的非金属在p区,金属铝、镓等都在p区;
C、铬价电子排布为3d54s1;
D、铜价电子排布为3d104s1.
解答 解:A、s区元素除氢元素外,都是金属元素,故A错误;
B、除氢外所有的非金属在p区,金属铝、镓等都在p区,所以p区不全部是非金属元素,故B错误;
C、铬价电子排布为3d54s1,不符合(n-1)d1~10ns2,故C错误;
D、铜价电子排布为3d104s1,而锌最后排4s上,所以除ds区外,故D正确;
故选D.
点评 本题考查结构与物质关系,难度不大,注意掌握元素周期表中各区的划分.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
19.下表中,对陈述I、II的正确性及两者间有无因果关系的判断都正确的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 用锌和足量稀硫酸制取氢气时加入硫酸铜溶液 | 可以加快制取氢气的速度 | Ⅰ对、Ⅱ对、无 |
| B | 用Mg-Al-NaOH构成原电池 | Mg更活泼作负极 | Ⅰ对、Ⅱ对、无 |
| C | 石墨常用做电解池的电极 | 石墨的化学性质稳定且导电性好 | Ⅰ对、Ⅱ对、有 |
| D | MgCl2是离子化合物 | 电解MgCl2的饱和溶液制取金属镁 | Ⅰ对、Ⅱ对、有 |
| A. | A | B. | B | C. | C | D. | D |
20.可以证明可逆反应N2+3H2?2NH3已达到平衡状态的是( )
①一个N≡N键断裂的同时,有3个H-H键断裂
②一个N≡N键断裂的同时,有6个N-H键断裂
③其它条件不变时,混合气体平均相对分子质量不再改变
④保持其它条件不变时,体系压强不再改变⑤NH3%、N2%、H2%都不再改变.
①一个N≡N键断裂的同时,有3个H-H键断裂
②一个N≡N键断裂的同时,有6个N-H键断裂
③其它条件不变时,混合气体平均相对分子质量不再改变
④保持其它条件不变时,体系压强不再改变⑤NH3%、N2%、H2%都不再改变.
| A. | 全部 | B. | 只有①③④⑤ | C. | ②③④⑤ | D. | 只有①③⑤ |
4.有关l3C、15N的下列说法正确的是( )
| A. | 13C与15N有相同的中子数 | B. | 13C与C60互为同素异形体 | ||
| C. | 15N与14N互为同位素 | D. | 15N和14N的化学性质不同 |
14.下列离子方程式书写正确是( )
| A. | 氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ | |
| B. | 将少量氯化铁溶液滴入硫化钠溶液中:2Fe3++S2-=2Fe2++S↓ | |
| C. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO | |
| D. | 向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
1.下列物质中,能在空气中稳定保存的是( )
| A. | NaOH固体 | B. | 稀H2SO4 | C. | Na2SO3晶体 | D. | 水玻璃 |
18.要加快H2O2分解的速度,下列措施不可行的是( )
| A. | 加热或光照 | B. | 加MnO2或FeCl3 | C. | 加压 | D. | 增大H2O2的浓度 |
19.下列关于化学反应中的能量变化的表述正确的是( )
| A. | 加热才能发生的反应一定是吸热反应 | |
| B. | 断开化学键的过程会吸收能量 | |
| C. | 化学能不仅可以与热能相互转化,还可以与电能相互转化 | |
| D. | 燃烧可能为吸热反应 |
 与NaOH的醇溶液共热制备CH3-CH═CH2
与NaOH的醇溶液共热制备CH3-CH═CH2 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备