题目内容
6.下列混合溶液中,各离子浓度的大小顺序不正确的是( )| A. | 物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+c(CH3COOH)=2c(Na+) | |
| B. | 物质的量浓度相等Na2CO3和NaHCO3溶液等体积混合:离子浓度的大小顺序是:c (Na+)>c (HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| C. | CH3COONa溶液中c(OH-)=c(CH3COOH)+c(H+) | |
| D. | 1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
分析 A.根据混合液中的物料守恒分析;
B.碳酸根离子的水解程度大于碳酸氢根离子,溶液呈碱性,据此进行判断各离子浓度大小;
C.根据醋酸钠溶液中的质子守恒判断;
D.根据碳酸钠溶液中的质子守恒判断.
解答 解:A.等体积等物质的量浓度的CH3COOH与CH3COONa混合,根据物料守恒可得:c(CH3COO-)+c(CH3COOH)=2c(Na+),故A正确;
B.物质的量浓度相等Na2CO3和NaHCO3溶液等体积混合,由于碳酸根离子的水解程度大于碳酸氢根离子,溶液呈碱性,则:c (HCO3-)>c(CO32-)、c(OH-)>c(H+),溶液中离子浓度的大小顺序是:c (Na+)>c (HCO3-)>c(CO32-)>c(OH-)>c(H+),故B正确;
C.CH3COONa溶液中,根据质子守恒可得:c(OH-)=c(CH3COOH)+c(H+),故C正确;
D.1mol/LNa2CO3溶液,根据质子守恒可得:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3),故D错误;
故选D.
点评 本题考查了离子浓度大小比较,题目难度中等,注意掌握盐的水解原理及其应用方法,明确电荷守恒、物料守恒及质子守恒的含义为解答关键,试题侧重考查学生的分析能力及灵活应用能力.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
16.有关高温结构陶瓷和光导纤维说法不正确的是( )
| A. | 光导纤维是一种能高质量传导光的玻璃纤维 | |
| B. | 光导纤维的抗干扰性能好,不发生电辐射,通讯质量高,能防窃听 | |
| C. | 高温结构陶瓷弥补了金属材料的弱点,但是硬度却远远低于金属材料 | |
| D. | 氮化硅陶瓷是一种重要的结构材料,具有超硬性,它能与氢氟酸反应 |
17.下列各原子或离子的电子排布式错误的是( )
| A. | Si 1s22s22p2 | B. | O2- 1s22s22p6 | ||
| C. | Na+ 1s22s22p6 | D. | Al 1s22s22p63s23p1 |
1.以下实验方法肯定错误的是( )
| A. | 判断H2O2分解速率的大小,可以通过测定单位时间内H2O2分解放出的O2的体积 | |
| B. | 制摩尔盐时用酒精洗涤产品 | |
| C. | 用米汤直接检验食用盐中是否含有碘元素 | |
| D. | 以硝酸钠和氯化钾为原料可以制备硝酸钾 |
11.同一周期的4种元素,原子半径从小到大的顺序为C<A<D<B(不包括稀有气体元素),则最有可能形成共价化合物的是( )
| A. | C与A | B. | C与D | C. | D与B | D. | B与C |
18.现有部分短周期元素的性质或原子结构如下表:
(1)元素T位于元素周期表的第三周期第ⅥA族.写出T2-的原子结构示意图 .
.
(2)元素Y氢元素形成一种离子YH4+,写出该微粒发生水解反应的离子方程式NH4++H2O?NH3.H2O+H+.
(3)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a 常温下Z的单质和T的单质状态不同
b Z的氢化物比T的氢化物稳定
c 一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一.T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是H2CO3(填化学式).
| 元素编号 | 元素性质或原子结构 |
| T | M层电子数比K层电子数多4个 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
 .
.(2)元素Y氢元素形成一种离子YH4+,写出该微粒发生水解反应的离子方程式NH4++H2O?NH3.H2O+H+.
(3)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a 常温下Z的单质和T的单质状态不同
b Z的氢化物比T的氢化物稳定
c 一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一.T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是H2CO3(填化学式).
15.化学反应H2+Cl2═2HCl的能量变化如图所示,则下列说法正确的是( )
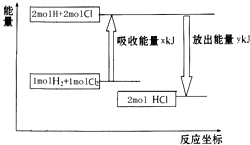

| A. | 该反应是放热反应 | |
| B. | 断裂1 mol H-H键和1 mol Cl-Cl 键放出x kJ能量 | |
| C. | 断裂1 mol H-Cl键需要吸收y kJ的能量 | |
| D. | 2 mol HCl的总能量高于1 mol H2和1 molCl2的总能量 |
16.下列有关纤维素的叙述正确的是( )
| A. | 纤维素在稀硫酸、加热的条件下水解 | |
| B. | 棉制品吸湿性好和分子中具有-OH有关 | |
| C. | 纤维指的就是纤维素 | |
| D. | 纤维素因分子结构中含-OH,可和浓HNO3发生硝化反应 |