题目内容
14.下列反应中,属于放热反应的是②③④⑤⑥⑧,属于吸热反应的是①⑦(填序号).①煅烧石灰石(主要成分CaCO3)制取生石灰(CaO) ②燃烧木炭取暖 ③炸药爆炸④酸与碱中和反应 ⑤食物因氧化而腐败 ⑥生石灰与水作用制熟石灰⑦Ba(OH)2•8H2O晶体与NH4Cl晶体⑧金属钠与水的反应.
分析 化学上把有热量放出的反应叫做放热反应,燃烧反应、中和反应等都是放热反应;把吸收热量的反应叫做吸热反应,一般分解反应、有碳参与的氧化还原反应、消石灰与氯化铵固体反应等是吸热反应.
解答 解:①煅烧石灰石制生石灰(CaO)是分解反应,则属于吸热反应,
②燃烧木炭是放热反应,
③炸药爆炸是放热反应,
④酸与碱中和反应是放热反应,
⑤食物因氧化而腐败是放热反应,
⑥生石灰与水作用制熟石灰是放热反应,
⑦Ba(OH)2•8H2O晶体与NH4Cl晶体属于吸热反应,
⑧金属钠与水的反应是放热反应.
故答案为:②③④⑤⑥⑧;①⑦.
点评 此题是对放热吸热反应的考查,解题的关键是熟记教材提到的几个反应就可以.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.X+、Y2+、Z3+、W2-均为第三周期元索的简单离子,其中不影响水的电离平衡的微粒是( )
| A. | X+ | B. | Y2+ | C. | Z3+ | D. | W2- |
5.下列溶液均处于25℃,有关叙述正确的是( )
| A. | 某物质的水溶液PH<7,则该物质一定是酸或强酸弱碱盐 | |
| B. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 | |
| C. | 稀释醋酸溶液,溶液中所有离子的浓度均降低 | |
| D. | pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-) |
2.下列有关σ键的说法错误的是( )
| A. | 如果电子云图象是由两个s电子重叠形成的,即形成s-sσ键 | |
| B. | s电子与p电子形成s-pσ键 | |
| C. | p电子和p电子不能形成σ键 | |
| D. | HCl分子里含有一个s-pσ键 |
6.聚丙烯酸酯的结构为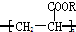 ,下列有关它的说法中,不正确的是( )
,下列有关它的说法中,不正确的是( )
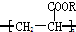 ,下列有关它的说法中,不正确的是( )
,下列有关它的说法中,不正确的是( )| A. | 它可由CH2=CH-COOR经加成聚合反应得到 | |
| B. | 在一定条件下能发生加成反应 | |
| C. | 聚丙烯酸酯材料是一种混合物 | |
| D. | 聚丙烯酸酯是高分子化合物 |
3.两种气态烃以任意比例混合,在105℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L,有下列组合的混合烃①C2H4和C3H4 ②CH4和C2H4 ③CH4和C4H4 ④C2H2和C3H4
其中符合上述要求的是( )
其中符合上述要求的是( )
| A. | 只有② | B. | 只有②④ | C. | 只有②③④ | D. | 只有①②③ |
4.有部分元素的性质与原子(或分子)结构如下表:
(1)写出元素T的原子结构示意图: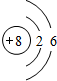 .
.
(2)元素Y与元素Z相比,金属性较强的是Na(用元素符号表示).下列表述中能证明这一事实的是cd(填序号).
a.Y单质的熔点比Z单质低 b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈 d.Y最高价氧化物对应的水化物的碱性比Z强
(3)写出T与Y形成的化合物的化学式Na2O,Na2O2.
(4)元素T和氢元素以原子个数比1:1化合形成化合物Q,元素X与氢元素以原子个数比1:2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式:N2H4+2H2O2═N2↑+4H2O.
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第三周期元素的简单离子中半径最小 |
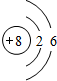 .
.(2)元素Y与元素Z相比,金属性较强的是Na(用元素符号表示).下列表述中能证明这一事实的是cd(填序号).
a.Y单质的熔点比Z单质低 b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈 d.Y最高价氧化物对应的水化物的碱性比Z强
(3)写出T与Y形成的化合物的化学式Na2O,Na2O2.
(4)元素T和氢元素以原子个数比1:1化合形成化合物Q,元素X与氢元素以原子个数比1:2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式:N2H4+2H2O2═N2↑+4H2O.
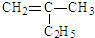
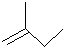
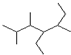 的名称2,3,5-三甲基-4-乙基庚烷
的名称2,3,5-三甲基-4-乙基庚烷 ②氢氧根离子
②氢氧根离子
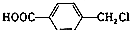 水解制得,写出K在浓硫酸作用下生成的聚合物的结构简式
水解制得,写出K在浓硫酸作用下生成的聚合物的结构简式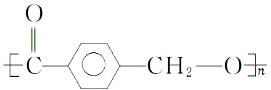 .
.