题目内容
3.两种气态烃以任意比例混合,在105℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L,有下列组合的混合烃①C2H4和C3H4 ②CH4和C2H4 ③CH4和C4H4 ④C2H2和C3H4其中符合上述要求的是( )
| A. | 只有② | B. | 只有②④ | C. | 只有②③④ | D. | 只有①②③ |
分析 有机物燃烧前后体积不变,可设有机物的平均式为CxHy,根据燃烧的方程式CxHy+(x+$\frac{y}{4}$)O2→xCO2+$\frac{y}{2}$H2O可知:1+x+$\frac{y}{4}$=x+$\frac{y}{2}$,解得:y=4,
即:混合气中平均含有H原子数为4,据此进行判断.
解答 解:设有机物的平均式为CxHy,则有:CxHy+(x+$\frac{y}{4}$)O2→xCO2+$\frac{y}{2}$H2O,有机物燃烧前后总体积不变,则
1+x+$\frac{y}{4}$=x+$\frac{y}{2}$,解得:y=4,
即:混合气中平均含有H原子数为4,
①C2H4和C3H4中H原子数都为4,平均值为4,符合题意,故①正确;
②CH4、C2H4中H原子数都是4,平均,为4,符合条件,故②正确;
③CH4和C4H4中H原子数都为4,平均值为4,符合题意,故③正确;
④C2H2、C3H4H原子数分别为2、4,平均H原子数不可能为4,故④错误;
所以符合条件的为①②③,
故选D.
点评 本题考查了混合物反应的计算,题目难度中等,注意根据有机物燃烧的方程式,用平均值法进行计算,试题侧重考查学生的分析能力及化学计算能力.

练习册系列答案
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目
13.设NA为阿伏伽德罗常数的值,下列说法错误的是( )
| A. | 0.1molMg2+含有NA个电子 | |
| B. | 1mol•L-1的NaCl溶液中含有NA个Na+ | |
| C. | 2molCu与足量S加热充分反应,转移2NA个电子 | |
| D. | 4gCH4与Cl2在光照条件下反应全部转化为CCl4时,断裂NA个C-H键 |
11.下列各组物质气化或熔化时,所克服的微粒间的作用力,属同种类型的是( )
| A. | 氯化钠和铁的熔化 | B. | 二氧化硅和生石灰的熔化 | ||
| C. | 碘和干冰的升华 | D. | 食盐和冰的熔化 |
18.把a,b,c三块金属片浸入稀硫酸中,用导线两两相连组成原电池,若a,b相连时,a为负数;b,c相连时,电子由c经导线流向b;a,c相连时,c极上产生大量气泡,则三种金属的活动性由强到弱的顺序为( )
| A. | a>b>c | B. | a>c>b | C. | c>a>b | D. | c>b>a |
8.下列选用的相关仪器及基本操作符合实验要求的是( )
| A. | 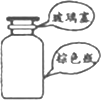 存放浓硝酸 | B. |  向试管中滴加液体 | ||
| C. |  称量NaOH固体 | D. | 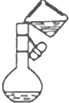 配制溶液时转移溶液 |
13.NA为阿伏加德罗常数,下列有关说法中正确的是( )
| A. | 2.3 g Na被O2完全氧化生成Na2O和Na2O2混合物时,失去电子数为0.1~0.2 NA | |
| B. | 常温下,64 g SO2所含的氧原子数为2NA | |
| C. | 标准状况下,等物质的量的SO2和SO3所占体积相同 | |
| D. | 100 mL 0.1 mol•L-1的硫酸铝溶液中含有的Al3+为0.02NA个 |
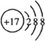 ;
;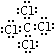 ,分子内含有极性键.
,分子内含有极性键.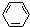 、④HCHO.其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质)加成产物CH3OH分子之间能形成氢键.
、④HCHO.其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质)加成产物CH3OH分子之间能形成氢键.