题目内容
9.下列说法错误的是( )| A. | 分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 | |
| B. | 能自发进行的化学反应,焓变和熵变一定符合:△H<0、△S>0 | |
| C. | 将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为纯碱 | |
| D. | 用FeCl3饱和溶液制Fe(OH)3胶体的过程属于吸热过程 |
分析 A.分散系中分散质小于1nm的是溶液,大于100nm的是浊液,介于1-100nm的是胶体;
B.反应能否自发进行应看△H-T△S数值是否小于O;
C.碳酸氢钠不稳定加热易分解生成碳酸钠;
D.盐类水解是吸热反应.
解答 解:A.分散系中分散质小于1nm的是溶液,大于100nm的是浊液,介于1-100nm的是胶体,所以Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液,故A正确;
B.反应能否自发进行应看△H-T△S数值,只有△H-T△S<0的反应才能自发进行,△H<0、△S>0,△H-T△S不一定小于0,反应不一定自发进行,故B错误;
C.碳酸氢钠不稳定加热易分解生成碳酸钠,将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为碳酸钠,故C正确;
D.FeCl3饱和溶液水解生成Fe(OH)3胶体,盐类水解是吸热反应,故D正确;
故选B.
点评 本题考查了分散系的分类,反应自发进行的判据,盐类的水解,电解的原理,题目综合性比较强,难度中等,注意B选项,反应自发进行的判据.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列叙述正确的是( )
| A. | 硅酸、氯化铁均为胶体 | B. | 醋酸、蔗糖均属于电解质 | ||
| C. | 水玻璃、氯水均为混合物 | D. | 氧化钙、氧化铝均为碱性氧化物 |
14.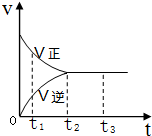 在一密闭容器中放入1mol X,进行可逆反应2X(g)?3Y(g),反应过程中的反应速率(v)与时间(t)的变化关系如图所示,下列叙述正确的是( )
在一密闭容器中放入1mol X,进行可逆反应2X(g)?3Y(g),反应过程中的反应速率(v)与时间(t)的变化关系如图所示,下列叙述正确的是( )
 在一密闭容器中放入1mol X,进行可逆反应2X(g)?3Y(g),反应过程中的反应速率(v)与时间(t)的变化关系如图所示,下列叙述正确的是( )
在一密闭容器中放入1mol X,进行可逆反应2X(g)?3Y(g),反应过程中的反应速率(v)与时间(t)的变化关系如图所示,下列叙述正确的是( )| A. | t1时,只有正反应在进行 | |
| B. | t2~t3时间段,反应停止 | |
| C. | t2时,容器内有1.5mol Y | |
| D. | t2~t3时间段,X,Y的物质的量均没有发生变化 |
1.标准状况下两种等物质的量的可燃气体共1.68L,其中一种是烃,在足量氧气中完全燃烧.若将产物通入足量澄清石灰水,得到的白色沉淀质量为15.0g;若用足量碱石灰吸收燃烧产物,增重9.3g.则这两种混合气体可能为( )
| A. | H2与C2H4 | B. | CO与C2H4 | C. | H2与C4H6 | D. | CO 与C3H6 |
18.下列物质的类别与所含官能团都正确的是( )
| A. | 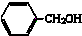 酚类-OH 酚类-OH | B. | 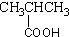 羧酸-CHO 羧酸-CHO | C. |  醛类-CHO 醛类-CHO | D. | CH3-O-CH3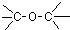 |
19.下列对于二氯二溴甲烷(CCl2Br2 )的认识正确的是( )
| A. | 只有一种结构 | B. | 有两种同分异构体 | ||
| C. | 属于烷烃 | D. | 属于正四面体结构 |