题目内容
4.下列叙述正确的是( )| A. | 硅酸、氯化铁均为胶体 | B. | 醋酸、蔗糖均属于电解质 | ||
| C. | 水玻璃、氯水均为混合物 | D. | 氧化钙、氧化铝均为碱性氧化物 |
分析 A.分散质微粒直径在1-100nm的分散系属于胶体;
B.水溶液中或熔融状态下能够导电的化合物称为电解质;
C.两种或多种物质组成的为混合物;
D.碱性氧化物指与水反应只生成碱,或与酸反应只生成盐和水的氧化物.
解答 解:A.硅酸是纯净物,不属于胶体,氯化铁也不是胶体,故A错误;
B.蔗糖在水溶液中和熔融状态下都不能够本身电离而导电,是非电解质,不是电解质,故B错误;
C.水玻璃是硅酸钠溶液,氯水是氯气溶于水后混合物,它们都是混合物,故C正确;
D.氧化铝既能与酸反应又能与碱反应,为两性氧化物,故D错误.
故选C.
点评 本题考查了物质的分类的方法应用,明确物质的组成是解题关键,题目较简单.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
14.7.4g某饱和一元醇X与足量金属Na反应,产生标准状况下H2 1.12L,则饱和一元醇X的可能结构有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
12.含有下列离子的溶液中分别加入NaOH固体,能引起该离子浓度减小(溶液体积不变)的是( )
| A. | Cl- | B. | CO32- | C. | HCO3- | D. | AlO2- |
19.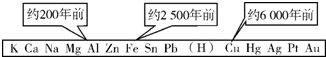 从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平.如图表示了三种金属被人类开发利用的大致年限,金属被利用年限的先后主要取决于( )
从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平.如图表示了三种金属被人类开发利用的大致年限,金属被利用年限的先后主要取决于( )
 从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平.如图表示了三种金属被人类开发利用的大致年限,金属被利用年限的先后主要取决于( )
从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平.如图表示了三种金属被人类开发利用的大致年限,金属被利用年限的先后主要取决于( )| A. | 金属的导电性强弱 | B. | 金属在地壳中的含量多少 | ||
| C. | 金属的化合价高低 | D. | 金属的活动性强弱 |
9.下列说法错误的是( )
| A. | 分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 | |
| B. | 能自发进行的化学反应,焓变和熵变一定符合:△H<0、△S>0 | |
| C. | 将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为纯碱 | |
| D. | 用FeCl3饱和溶液制Fe(OH)3胶体的过程属于吸热过程 |
13.下列有关化学用语正确的是( )
| A. | 乙烯的最简式C2H4 | B. | 乙醇的结构简式C2H6O | ||
| C. | 苯的分子式C6H6 | D. | 四氯化碳的电子式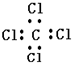 |
14.下列递变规律不正确的是( )
| A. | Na、Mg、Al还原性依次减弱 | |
| B. | F2、Cl2、Br2、I2单质的氧化性依次减弱 | |
| C. | C、N、O原子半径依次增大 | |
| D. | P、S、Cl最高正价依次升高 |
 某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl.
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl.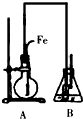 某学生用如图所示装置证明溴和苯的反应是取代反应而不是加成反应,主要实验步骤如下:
某学生用如图所示装置证明溴和苯的反应是取代反应而不是加成反应,主要实验步骤如下: