题目内容
17.用NA表示阿佛加德罗常数,下列说法中正确的是( )| A. | 1摩铜作还原剂一定提供NA个电子 | |
| B. | 64克二氧化硫中含有NA个氧分子 | |
| C. | 标准状况下,22.4升氨气中含有3NA个氢原子 | |
| D. | 18克重水中含有10NA个电子 |
分析 A、反应后铜元素可能变为+2价,也可能变为+1价;
B、二氧化硫中无氧气分子;
C、求出氨气的物质的量,然后根据1mol氨气中含3mol氢原子来计算;
D、重水的摩尔质量为20g/mol.
解答 解:A、反应后铜元素可能变为+2价,也可能变为+1价,故1mol铜做还原剂可能提供2mol电子也可能提供1mol电子,故A错误;
B、二氧化硫中无氧气分子,含的是氧原子,故B错误;
C、标况下,22.4L氨气的物质的量为1mol,而氨气中含3mol氢原子,即含3NA个,故C正确;
D、重水的摩尔质量为20g/mol,故18g重水的物质的量为0.9mol,而1mol重水中含10mol电子,故0.9mol重水含9mol电子,即9NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
7.下列过程吸收能量的是( )
| A. | 钠与水反应 | B. | H+H→H2 | C. | 石灰石分解 | D. | 酸碱中和 |
8.如图各装置能构成原电池的是( )
| A. | 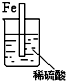 | B. | 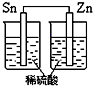 | C. | 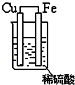 | D. | 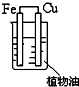 |
5.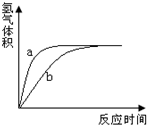 将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )
将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )
 将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )
将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )| A. | a表示水,b表示无水乙醇 | B. | a表示无水乙醇,b表示水 | ||
| C. | 都可用a曲线表示 | D. | 都可用b曲线表示 |
12.氮气化学性质稳定的原因是 ( )
| A. | 氮的非金属性弱 | B. | 氮气的熔沸点低 | ||
| C. | 氮原子半径较小 | D. | 氮分子中原子间共价键不易断裂 |
2.下列试剂保存方法错误的是( )
| A. | 少量白磷保存在水里 | |
| B. | 钠保存在煤油里 | |
| C. | 液溴保存在棕色玻璃瓶里且覆盖一层水 | |
| D. | 装氢氟酸的玻璃瓶用橡皮塞 |
9.常温下,分别将四块形状相同,质量为7g的铁块同时投入下列四种溶液中,生成氢气速率最快的是( )
| A. | 200 mL 2 mol•L-1HCl | B. | 100 mL 2 mol•L-1H2SO4 | ||
| C. | 100 mL 3 mol•L-1 HCl | D. | 50 mL 18.4 mol•L-1H2SO4 |
7.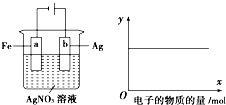 按图实验,若x轴表示流入阴极电子的物质的量,则y轴可表示①c(Ag+) ②c(NO3-)③a棒的质量④b棒的质量( )
按图实验,若x轴表示流入阴极电子的物质的量,则y轴可表示①c(Ag+) ②c(NO3-)③a棒的质量④b棒的质量( )
 按图实验,若x轴表示流入阴极电子的物质的量,则y轴可表示①c(Ag+) ②c(NO3-)③a棒的质量④b棒的质量( )
按图实验,若x轴表示流入阴极电子的物质的量,则y轴可表示①c(Ag+) ②c(NO3-)③a棒的质量④b棒的质量( )| A. | ①③ | B. | ③④ | C. | ①②④ | D. | ①② |
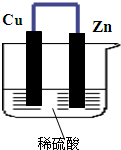 如图所示,将锌、铜通过导线相连,置于稀硫酸中.
如图所示,将锌、铜通过导线相连,置于稀硫酸中.