题目内容
9.常温下,分别将四块形状相同,质量为7g的铁块同时投入下列四种溶液中,生成氢气速率最快的是( )| A. | 200 mL 2 mol•L-1HCl | B. | 100 mL 2 mol•L-1H2SO4 | ||
| C. | 100 mL 3 mol•L-1 HCl | D. | 50 mL 18.4 mol•L-1H2SO4 |
分析 铁与盐酸、稀硫酸反应的本质为Fe+2H+=Fe2++H2↑,铁块相同时,H+离子浓度越大,反应速率越快,与溶液体积无关,常温下铁与浓硫酸钝化.
解答 解:A、2mol/LHCl,H+离子为2mol/L;
B、2mol/LH2SO4,H+离子为4mol/L;
C、3mol/LHCl,H+离子为3mol/L;
D、常温下铁与浓硫酸钝化,
所以,铁与2mol/LH2SO4反应最快.
故选B.
点评 本题考查了影响化学反应速率的因素,难度不大,易错选项是D,注意并不是浓度越大,化学反应速率越大,如D选项,因发生钝化现象而阻止反应发生.

练习册系列答案
相关题目
19.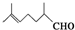 甜瓜醛是调制西瓜、甜瓜、黄瓜、柠檬、苹果等味道的食用香精.其结构简式如图所示.下列有关甜瓜醛的叙述正确的是( )
甜瓜醛是调制西瓜、甜瓜、黄瓜、柠檬、苹果等味道的食用香精.其结构简式如图所示.下列有关甜瓜醛的叙述正确的是( )
 甜瓜醛是调制西瓜、甜瓜、黄瓜、柠檬、苹果等味道的食用香精.其结构简式如图所示.下列有关甜瓜醛的叙述正确的是( )
甜瓜醛是调制西瓜、甜瓜、黄瓜、柠檬、苹果等味道的食用香精.其结构简式如图所示.下列有关甜瓜醛的叙述正确的是( )| A. | 该物质最多可与1 mol氢气发生加成反应 | |
| B. | 该物质的分子式为C9H14O | |
| C. | 加热条件下,该物质能与新制Cu(OH)2悬浊液反应 | |
| D. | 该物质为烯烃 |
20.下列烷烃化合物中,只有两种同分异构体的是( )
| A. | C2H6 | B. | C3H8 | C. | C4H10 | D. | C5H12 |
17.用NA表示阿佛加德罗常数,下列说法中正确的是( )
| A. | 1摩铜作还原剂一定提供NA个电子 | |
| B. | 64克二氧化硫中含有NA个氧分子 | |
| C. | 标准状况下,22.4升氨气中含有3NA个氢原子 | |
| D. | 18克重水中含有10NA个电子 |
4.有机物分子结构中基团之间的相互影响会导致物质化学性质的改变,下列各项的事实不能说明上述观点的是( )
| A. | 甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能 | |
| B. | 乙醇电离出H+的能力不及H2O | |
| C. | 乙烯能发生加成反应,而乙烷不能发生加成反应 | |
| D. | 苯酚能与NaOH溶液反应,而乙醇不能与NaOH溶液反应 |
14.在一定温度下,某固定容积的密闭容器中发生如下反应2NO2?2NO+O2.此反应达到平衡状态的标志是( )
| A. | NO2、NO、O2的物质的量浓度之比为2:2:1 | |
| B. | 单位时间内生成n mol O2,同时消耗2n mol NO2 | |
| C. | 混合气体的平均摩尔质量不再改变 | |
| D. | 正反应和逆反应都已停止 |
18.已知碳碳单键可以绕键轴自由旋转,结构简式为如图所示的烃,下列说法中正确的是( )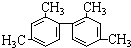

| A. | 分子中至少有12个碳原子处于同一平面上 | |
| B. | 分子中至少有10个碳原子处于同一平面上 | |
| C. | 分子中至少有11个碳原子处于同一平面上 | |
| D. | 该烃属于苯的同系物 |
19.下列气体既能用浓硫酸干燥又能用碱石灰干燥的是( )
| A. | SO2 | B. | NH3 | C. | N2 | D. | CO2 |
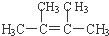 ;
;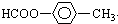
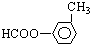
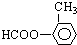 还有:
还有: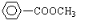 .
. .
.