题目内容
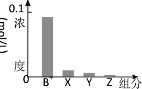
【题目】室温下,0.2mol/L的一元碱BOH与等浓度的盐酸等体积混合后,所得溶液中部分微粒的组分及浓度如图所示,下列对混合溶液的分析正确的是
A.溶液显酸性
B.升温,c(X)增大,c(Y)减小
C.c(B+) + c(Y) = c(Cl-)
D.稀释溶液,c(X)增大,c(Z)增大
【答案】AC
【解析】
![]() 的一元碱BOH与等浓度的盐酸等体积混合后,
的一元碱BOH与等浓度的盐酸等体积混合后,![]() ,所得溶液中
,所得溶液中![]() 浓度小于
浓度小于![]() ,说明在溶液中存在
,说明在溶液中存在![]() ,B0H为弱碱,BCl溶液呈酸性,则
,B0H为弱碱,BCl溶液呈酸性,则![]() ,一般来说,盐类的水解程度较小,则:
,一般来说,盐类的水解程度较小,则:![]() ,反应后溶液中离子浓度大小为:
,反应后溶液中离子浓度大小为:![]() 即X表示
即X表示![]() ,Y表示BOH,Z表示
,Y表示BOH,Z表示![]() ,溶液中存在物料守恒为:
,溶液中存在物料守恒为:![]() ,据此回答。
,据此回答。
A.BOH为弱碱,反应生成强酸弱碱盐BCl,则溶液显酸性,A正确;
B.盐的水解为吸热反应,升温促进水解,则Y浓度增大,B错误;
C.X表示![]() ,Y表示BOH,Z表示
,Y表示BOH,Z表示![]() ,溶液中存在物料守恒为:
,溶液中存在物料守恒为:![]() ,C正确;
,C正确;
D.稀释后促进水解,但是溶液中氢离子浓度减小,即![]() 减小,D错误;
减小,D错误;
答案选AC。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】氮的氧化物是严重的大气污染物,可以通过以下方法处理:
Ⅰ.催化还原法:如在汽车排气管上安装一个催化转化器,发生如下反应: 2NO(g)+2CO(g)N2(g)+2CO2(g)
(1)已知N2(g)+O2(g)2NO(g) △H=+180kJ/mol
化学键 | O=O | C=O | C≡O |
键能(kJ/mol) | 497 | 803 | 1072 |
则反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H=_____kJ/mol。
(2)在一定温度下,向体积为1L的密闭容器中充入2molNO、1molCO,10分钟时反应2NO(g)+2CO(g)N2(g)+2CO2(g)达到平衡状态,反应过程中反应物浓度随时间变化情况如图所示:
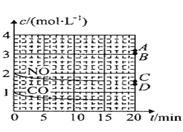
①该反应的平衡常数 K 的计算式为_____;前 10 分钟内用氮气表示的反应速率为_____。
②若保持温度不变,15 分钟时再向该容器中充入1.6molNO、0.4molCO2,则此时反应的ν正______ν逆(填“>”、“=”或“<”)。
③若保持其他条件不变,15min 时压缩容器的体积至 0.5L,20 分钟时反应重新达到平衡,NO 的浓度对应的点应是图中的_____(填字母)。
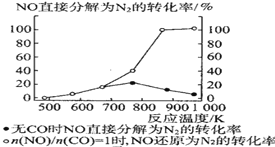
④某科研小组研究发现以 Ag-ZSM-5 为催化剂,NO 转化为 N2 的转化率随温度变化情况如图所示。若不使用 CO,温度超过775K,发现NO的分解率降低,其可能的原因是__________________
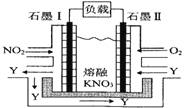
Ⅱ.利用电化学原理,将 NO2、O2和熔融 KNO3制成燃料电池,其原理如图,该电池在工作过程中NO2转变成绿色硝化剂Y,Y是一种氧化物,可循环使用,石墨Ⅰ附近发生的反应电极反应式为_____相同条件下,消耗的 O2和 NO2的体积比为_____