��Ŀ����
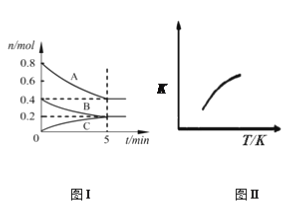
����Ŀ���̶��ݻ�Ϊ2 L���ܱ������з�����ӦxA(g)+yB(g) ![]() zC(g)��ͼI��ʾ200��ʱ�����и����ʵ�����ʱ��ı仯��ϵ��ͼII��ʾƽ��ʱƽ�ⳣ��K���¶ȱ仯�Ĺ�ϵ�����ͼ���жϣ����н�����ȷ����
zC(g)��ͼI��ʾ200��ʱ�����и����ʵ�����ʱ��ı仯��ϵ��ͼII��ʾƽ��ʱƽ�ⳣ��K���¶ȱ仯�Ĺ�ϵ�����ͼ���жϣ����н�����ȷ����
![]()
A. 200��ʱ����Ӧ�ӿ�ʼ��ƽ���ƽ����Ӧ����v(A)��0.08mol��L-1��min-1
B. ��0~5 minʱ�����������Ƚ�������Ϊm kJ����÷�Ӧ���Ȼ�ѧ����ʽ�ɱ�ʾΪ��2A + B ![]() C ��H = +5m kJ/mol
C ��H = +5m kJ/mol
C. 200��ʱ�����ڵ�6 min������ϵ�м���1molAr��A��ת���ʲ���
D. 200��ʱ��ƽ����ٳ���2 mol B��2 mol Cʱ��v����v��
���𰸡�C
��������
A�����ݻ�ѧ��Ӧ���ʵ���ѧ����ʽ��v(A)=(0.8��0.4)/(5��2)mol/(L��min)=0.04 mol/(L��min)����A����B����ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȵ������ʵ����仯֮�ȣ�x:y:z=(0.8��0.4):(0.4��0.2):0.2=2:1:1����Ӧ����ʽΪ2A(g)+ B(g) ![]() C(g)���¶����ߣ���ѧƽ�ⳣ�������˷�Ӧ����Ӧ�����ȷ�Ӧ���Ȼ�ѧ��Ӧ����ʽΪ2A(g)+ B(g)
C(g)���¶����ߣ���ѧƽ�ⳣ�������˷�Ӧ����Ӧ�����ȷ�Ӧ���Ȼ�ѧ��Ӧ����ʽΪ2A(g)+ B(g) ![]() C(g) ��H=��5mkJ��mol��1��Cѡ���Ȼ�ѧ��Ӧ����ʽû�б������ʵ�״̬����B����C������״̬�£�����Ƿ�Ӧ���壬���Ũ�Ȳ��䣬��A��ת���ʲ��䣬��C��ȷ��D�� 200��ʱ���ﵽƽ�⣬ƽ�ⳣ��K=
C(g) ��H=��5mkJ��mol��1��Cѡ���Ȼ�ѧ��Ӧ����ʽû�б������ʵ�״̬����B����C������״̬�£�����Ƿ�Ӧ���壬���Ũ�Ȳ��䣬��A��ת���ʲ��䣬��C��ȷ��D�� 200��ʱ���ﵽƽ�⣬ƽ�ⳣ��K=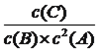 ��������ֵ�����K=25��ƽ����ٳ���2molB��2molC����ʱQc=25=K����ѧƽ�ⲻ�ƶ�����v��=v�棬��D����
��������ֵ�����K=25��ƽ����ٳ���2molB��2molC����ʱQc=25=K����ѧƽ�ⲻ�ƶ�����v��=v�棬��D����