题目内容
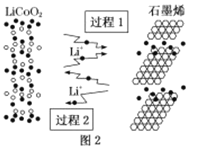
【题目】2019年10月9日,瑞典皇家科学院将2019年度诺贝尔化学奖授予美国JohnBGoodenough教授、M.stanleyWhittlingham教授和日本化学家AkiraYoshino,以表彰其在锂离子电池的发展方面作出的贡献。
(1)基态锂原子核外能量最高的电子所处能级的电子云轮廓图的形状为___;基态磷原子第一电离能比硫的___ (填“大”或“小”),原因是___。
(2)实室中可用KSCN或K4[Fe(CN)6]来检验Fe3+,FeCl3与KSCN溶液混合,可得到配位数为5的配合物的化学式是___;
(3)磷酸(H3PO4)和亚磷酸(H3PO3)是磷元素的两种含氧酸。PO43-的空间构型为___;亚磷酸与NaOH反应只生成NaHPO3和NaH2PO3两种盐,则H3PO3的结构式为___。
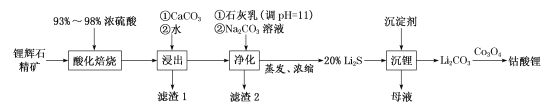
(4)磷酸分子间脱水可生成多磷酸,其某一钙盐的结构如图所示:
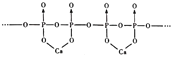
由图推知该多磷酸钙盐的通式为__(用n表示重复单元数)
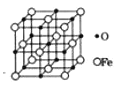
(5)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与O2-紧邻且等距离的Fe2+数目为__;Fe2+与O2-最短核间距为___pm。
【答案】球形 大 基态磷原子的3p轨道处于半充满状态,较稳定 K2[Fe(SCN)5] 正四面体 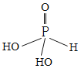 (CaP2O6)n 6
(CaP2O6)n 6 ![]() pm
pm
【解析】
(1)基态锂原子价电子排布式为2s1,电子最高占据2s能级,电子云轮廓图形为球形;基态磷原子的3p轨道处于半充满状态,较稳定,所以磷的第一电离能比硫大;
(2)Fe3+与SCN-形成的配合物中,Fe3+提供空轨道,SCN-提供孤对电子作为配体,所以配位数为5的配离子为[Fe(SCN)5]2-,相应的配合物的化学式是K2[Fe(SCN)5];
(3)PO43-中P的价层电子对数为4+![]() =4,无孤电子对,所以的空间构型为正四面体;亚磷酸H3PO3与NaOH反应只生成NaHPO3和NaH2PO3两种盐,说明亚磷酸含有2个羟基氢原子,另外的一个H、O直接与P相接,所以H3PO3的结构式为
=4,无孤电子对,所以的空间构型为正四面体;亚磷酸H3PO3与NaOH反应只生成NaHPO3和NaH2PO3两种盐,说明亚磷酸含有2个羟基氢原子,另外的一个H、O直接与P相接,所以H3PO3的结构式为 ;
;
(4)根据图知,其最小的重复部分为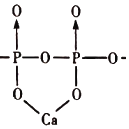 ,据此判断形成盐的化学通式为 (CaP2O6)n;
,据此判断形成盐的化学通式为 (CaP2O6)n;
(5)以体心O2-研究,与O2-紧邻且等距离的Fe2+处于面心,共有6个;Fe2+与O2-的最短核间距等于晶胞棱长的![]() ,晶胞中Fe2+数目=8×
,晶胞中Fe2+数目=8×![]() +6×
+6×![]() =4,O2-离子数目=1+12×
=4,O2-离子数目=1+12×![]() =4,所以晶胞质量=
=4,所以晶胞质量=![]() g,设二者最短距离为a pm,则晶胞棱长=2a pm,晶胞的体积为(2a×10-10cm)3=8a3×10-30cm3,则:
g,设二者最短距离为a pm,则晶胞棱长=2a pm,晶胞的体积为(2a×10-10cm)3=8a3×10-30cm3,则:![]() g=ρgcm-3×8a3×10-30cm3,解得a=
g=ρgcm-3×8a3×10-30cm3,解得a=![]() pm。
pm。

 阅读快车系列答案
阅读快车系列答案