题目内容
【题目】2019年诺贝尔化学奖颁给了日本吉野彰等三人,以表彰他们对锂离子电池研发的卓越贡献。
(1)工业中利用锂辉石(主要成分为LiAlSi2O6,还含有FeO、CaO、MgO等)制备钴酸锂(LiCoO2)的流程如图:
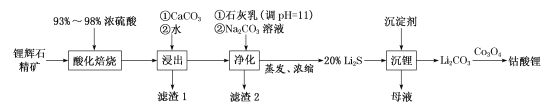
回答下列问题:
①锂辉石的主要成分为LiAlSi2O6,其氧化物的形式为___。
②为提高“酸化焙烧”效率,常采取的措施是___。
③向“浸出液”中加入CaCO3,其目的是除去“酸化焙烧”中过量的硫酸,控制pH使Fe3+、A13+完全沉淀,则pH至少为___。(已知:,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.0×10-33,完全沉淀后离子浓度低于1×l0-5)mol/L)。
④“滤渣2”的主要化学成分为___。
⑤“沉锂”过程中加入的沉淀剂为饱和的___(化学式)溶液。
(2)利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LiCoO2+C6![]() LixC6+Li1-xCoO2其工作原理如图2。下列关于该电池的说法正确的是___(填字母)。
LixC6+Li1-xCoO2其工作原理如图2。下列关于该电池的说法正确的是___(填字母)。
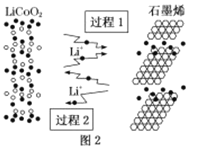
A.过程1为放电过程
B.该电池若用隔膜可选用质子交换膜
C.石墨烯电池的优点是提高电池的储锂容量进而提高能量密度
D.充电时,LiCoO2极发生的电极反应为LiCoO2-xe-=xLi++Li1-xCoO2
E.对废旧的该电池进行“放电处理”让Li+嵌入石墨烯中而有利于回收
(3)LiFePO4也是一种电动汽车电池的电极材料,实验室先将绿矾溶解在磷酸中,再加入氢氧化钠和次氯酸钠溶液反应获得FePO4固体。再将FePO4固体与H2C2O4和LiOH反应即可获得LiFePO4同时获得两种气体。
①写出FePO4固体与H2C2O4和LiOH反应溶液获得LiFePO4的化学方程式___。
②LiFePO4需要在高温下成型才能作为电极,高温成型时要加入少量活性炭黑,其作用是___。
【答案】Li2OAl2O34SiO2 将矿石细磨、搅拌、升高温度 4.7 Mg(OH)2和CaCO3 Na2CO3 CD 2LiOH+6H2C2O4+2FePO4=2LiFePO4+7CO2↑+5CO↑+7H2O 与空气中的氧气反应,防止LiFePO4中的Fe2+被氧化
【解析】
锂辉石(主要成分为LiAlSi2O6,还含有FeO、CaO、MgO等)为原料来制取钴酸锂(LiCoO2),加入过量浓硫酸酸化焙烧锂辉矿,之后加入碳酸钙除去过量的硫酸,并使铁离子、铝离子沉淀完全,然后加入氢氧化钙和碳酸钠调节pH沉淀镁离子和钙离子,过滤得到主要含锂离子的溶液,滤液蒸发浓缩得20%Li2S,加入碳酸钠沉淀锂离子生成碳酸锂,洗涤后与Co3O4高温下焙烧生成钴酸锂;
(1)①硅酸盐改写成氧化物形式的方法如下:a.氧化物的书写顺序:活泼金属氧化物→较活发金属氧化物→二氧化硅→水,不同氧化物间以·隔开;b.各元素的化合价保持不变,且满足化合价代数和为零,各元素原子个数比符合原来的组成;c、当计量数配置出现分数时应化为整数;锂辉石的主要成分为LiAlSi2O6,根据方法,其氧化物的形式为Li2OAl2O34SiO2;
②流程题目中为提高原料酸侵效率,一般采用的方法有:减小原料粒径(或粉碎)、适当增加酸溶液浓度、适当升高温度、搅拌、多次浸取等;本题中为“酸化焙烧“,硫酸的浓度已经最大,因此合理的措施为将矿石细磨、搅拌、升高温度等;
③Al(OH)3的Ksp大于Fe(OH)3的Ksp,那么保证Al3+完全沉淀即可达到目的;已知Al(OH)3的Ksp=1×10-33,所以当c(Al3+)=1×10-5mol/L时可认为铝离子和铁离子完全沉淀,此时 c(OH-)=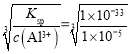 =mol/L=1×10-9.3mol/L,c(H+)=1×10-4.7mol/L,pH=4.7,即pH至少为4.7;
=mol/L=1×10-9.3mol/L,c(H+)=1×10-4.7mol/L,pH=4.7,即pH至少为4.7;
④根据分析可知滤渣2主要为Mg(OH)2和CaCO3;
⑤根据“沉锂”后形成Li2CO3固体,以及大量生产的价格问题,该过程中加入的最佳沉淀剂为Na2CO3溶液;
(2)A.电池反应式为LiCoO2+C6![]() LixC6+Li1-xCoO2,由此可知,放电时,负极电极反应式为LixC6-xe-=xLi++C6,正极电极反应式Li1-xCoO2+xLi++xe-=LiCoO2,石墨电极为放电时的负极,充电时的阴极,故A错误;
LixC6+Li1-xCoO2,由此可知,放电时,负极电极反应式为LixC6-xe-=xLi++C6,正极电极反应式Li1-xCoO2+xLi++xe-=LiCoO2,石墨电极为放电时的负极,充电时的阴极,故A错误;
B.该电池是利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性而制作,故B错误;
C.石墨烯电池利用的是Li元素的得失电子,因此其优点是在提高电池的储锂容量的基础上提高了能量密度,故C正确;
D.充电时,LiCoO2极为阳极,将放电时的正极电极反应式逆写即可得阳极反应,即LiCoO2极发生的电极反应为LiCoO2-xe-=xLi++Li1-xCoO2,故D正确;;
E.根据钴酸锂的制备流程可知,对废旧的该电池进行“放电处理“让Li+嵌入LiCoO2才有利于回收,故E错误;
故答案为CD;
(3)①FePO4固体与H2C2O4和LiOH反应可获得LiFePO4同时获得两种气体,该过程中Fe3+被还原,根据元素价态变化规律可知应是C元素被氧化,生成CO2,该种情况下只生成一种气体,应想到草酸不稳定容易发生歧化反应分解生成CO和CO2,即获得的两种气体为CO和CO2,结合电子守恒和元素守恒可能方程式为:2LiOH+6H2C2O4+2FePO4=2LiFePO4+7CO2↑+5CO↑+7H2O;
②高温条件下亚铁离子容易被空气中的氧气氧化,活性炭黑具有还原性,可以防止LiFePO4中的Fe2+被氧化。

【题目】CS2是一种常见溶剂,还可用于生产人造粘胶纤维等。回答下列问题:
(1)CS2与酸性KMnO4溶液反应,产物为CO2和硫酸盐,该反应中还原剂与氧化剂的物质的量之比为 _______(MnO4-被还原为Mn2+)
(2)甲烷硫磺法制取CS2的反应为CH4(g)+2S2(g)![]() CS2(g)+2H2S(g) △H。
CS2(g)+2H2S(g) △H。
① 在恒温恒容密闭容器中进行该反应时,能说明该反应已达到平衡状态的是_______(填字母)
A.v正(S2)=2v逆(CS2)
B.容器内气体的密度不再随时间变化
C.容器内气体的总压强不再随时间变化
D.单位时间内断裂C-H键数目与断裂H—S键数目相等
②已知下列键能数据:
共价键 | C—H | S=S | C=S | H—S |
律能/kJmol-1 | 411 | 425 | 573 | 363 |
该反应的△H _______kJmol-1
(3)在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S):n(CH4)=2:1,发生反应:CH4(g) +2H2S(g)CS2(g) + 4H2(g)。0.1MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:
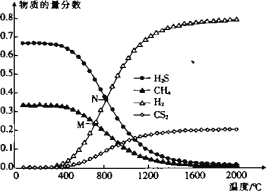
①该反应△H _______(填“>”或“<”)0。
②M点,H2S的平衡转化率为_______,为提高H2S的平衡转化率,除改变温度外,还可采取的措施是_______(列举一条)。
③N点,平衡分压p(CS2)=_______MPa,对应温度下,该反应的KP =_______(MPa)2。(KP为以分压表示的平衡常数)