��Ŀ����
����Ŀ���ϳ��뿪��������Ȼ�粢�����ڵ������ʡ��²��ϣ���Ϊ����������ִ���ѧ����Ҫ����������ѧ֪ʶ�ش��������⣺
(1)ɳ̲��ɳ������Ҫ�ɷ���____����ҵ�Ͽ���ɳ������Ҫ�ɷ��봿���ڸ����·�Ӧ�Ʊ�Na2SiO3���÷�Ӧ�Ļ�ѧ����ʽΪ____��
(2)��������ˮ��ɱ����������������ˮ�е�����ɫʯ����Һ��������___��������˵����ˮ�к���_______(�ѧʽ�����ӷ���)��
(3)ֱ����������Ư�������Ա��棬Ч�������롣���������ʵ�顢�Ľ���Ŀǰ���õ���Ư�ۡ���ҵ��ȡƯ�۵Ļ�ѧ����ʽΪ__��
���𰸡�SiO2 SiO2 + Na2CO3 ![]() Na2SiO3 + CO2�� �ȱ�����ɫ H+��ClO-��HClO��HCl 2Cl2+2Ca(OH)2 =CaCl2 + Ca(ClO)2 + 2H2O
Na2SiO3 + CO2�� �ȱ�����ɫ H+��ClO-��HClO��HCl 2Cl2+2Ca(OH)2 =CaCl2 + Ca(ClO)2 + 2H2O
��������
����SiO2�����ʼ������ι�ҵ���⣻����������ˮ��Ӧ�IJ��������ˮ�ijɷּ����ʣ�����������Ӧ��ԭ��������
(1)ɳ̲��ɳ������Ҫ�ɷ���SiO2��SiO2�봿���ڸ����·�Ӧ�Ʊ�Na2SiO3��������Ӧ�Ļ�ѧ����ʽΪSiO2 + Na2CO3![]() Na2SiO3 + CO2����
Na2SiO3 + CO2����
(2)��������ˮ����ˮ��Ӧ����HCl��HClO������HClO��ǿ����������������ˮ�е�����ɫʯ����Һ���������ȱ�����ɫ��������˵����ˮ�к���H+��ClO-��HClO��HCl��
(3)��ҵ������Cl2����ʯ�һ����ȡƯ�۵Ļ�ѧ����ʽΪ2Cl2+2Ca(OH)2 =CaCl2 + Ca(ClO)2 + 2H2O��

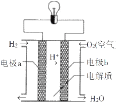
����Ŀ��ij��ѧ��ȤС��Ϊ��̽�����缫�ڵ���е����ã���Ʋ���������ʵ������¼����:
��� | �缫���� | �������Һ | ������ָ��ƫת���� |
1 | Al��Cu | ϡ���� | ƫ��Cu |
2 | Al��C��ʯī�� | ϡ���� | ƫ��ʯī |
�ش����У�1������2��С��:
��ʵ��1��Al���ĵ缫Ϊ____(��������������������)��Cu���ĵ缫Ϊ____(��������"����������)��
��ʵ��2�۲쵽C(ʯī)���ϲ�����������____,�����ĵ缫��ӦʽΪ____.��ͼ�ǵ����Ϊϡ������Һ������ȼ�ϵ�ء��õ�صĵ��Ӵӵ缫____������������缫____(��a��b)