题目内容
【题目】已知FeS溶于盐酸中,生成FeCl2和H2S气体。现将100mL2.0mol/L的盐酸加入到一定量的FeS固体中,以制备H2S气体。当盐酸完全反应后假定溶液体积不变。
试计算:(1)可收集到的H2S气体在标准状况下的体积___________________;
(2)反应后溶液中FeCl2的物质的量浓度_________________________。
【答案】2.24L 1mol/L
【解析】
FeS溶于盐酸中,生成FeCl2和H2S气体,发生反应的化学方程式为FeS + 2HCl = FeCl2 + H2S↑,结合原子守恒和浓度公式解题即可。
n(HCl) = c(HCl) ×V(溶液) = 2.0mol/L×0.1L=0.2mol,根据FeS + 2HCl = FeCl2 + H2S↑可知,生成的n(H2S) =0.1mol、n( FeCl2) = 0.1mol,则:
(1)可收集到的H2S气体在标准状况下的体积为0.1mol ×22.4L/mol=2.24L;
(2)反应后溶液中FeCl2的物质的量浓度c( FeCl2) =![]() = 1mol/L。
= 1mol/L。

 优学名师名题系列答案
优学名师名题系列答案【题目】I. 合成气(CO+H2)广泛用于合成有机物,工业上常采用天然气与水蒸气反应等方法来制取合成气。
(1)已知:5.6L(标况下)CH4与水蒸气完全反应,吸收51.5KJ的热量,请写出该反应的热化学方程式_______________________________________________。
(2)在150℃时2L的密闭容器中,将2 mol CH4和2 mol H2O(g)混合,经过15min达到平衡,此时CH4的转化率为60%。回答下列问题:
①从反应开始至平衡,用氢气的变化量来表示该反应速率v(H2)=____________。
②在该温度下,计算该反应的平衡常数K=________________________(保留两位小数)。
③下列选项中能表示该反应已达到平衡状态的是__________________________
A.v(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.C (CH4) = C (CO)
(3)合成气中的氢气也用于合成氨气:N2 + 3H2![]() 2NH3。保持温度和体积不变, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是___________。
2NH3。保持温度和体积不变, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是___________。
容 器 | 体积 | 起始物质 | 平衡时NH3的物质的量 | 平衡时N2的 体积分数 | 反应开始时的速率 | 平衡时容器内压强 |
甲 | 1L | 1molN2+3molH2 | 1.6mol | φ甲 | ν甲 | P甲 |
乙 | 1L | 2molN2+6molH2 | n1 mol | φ乙 | ν乙 | P乙 |
丙 | 2L | 2molN2+6molH2 | n2 mol | φ丙 | ν丙 | P丙 |
A.n1=n2=3.2 B.φ甲=φ丙>φ乙 C.ν乙>ν丙>ν甲 D.P乙>P甲=P丙
II.(1)常温下,在x mol·L-1氨水中加入等体积的y mol·L-1硫酸得混合溶液M恰好显中性。
①M溶液中所有离子浓度由大到小的顺序为_________________。
②常温下,NH3·H2O的电离常数K=_____(用含x和y的代数式表示,忽略溶液混合前后的体积变化)。
(2)利用电解法处理高温空气中稀薄的NO(O2浓度约为NO浓度的10倍),装置示意图如下,固体电解质可传导O2-
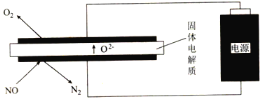
阴极的电极反应式为___________________________。
②消除一定量的NO所消耗的电量远远大于理论计算量,可能的原因是(不考虑物理因素)________。