题目内容
【题目】元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4—(绿色)、Cr2O72—(橙红色)、CrO42—(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答:
(1)Cr3+与Al3+的化学性质相似,往Cr2(SO4)3溶液中滴入NaOH溶液直至过量,可观察到的现象是 。
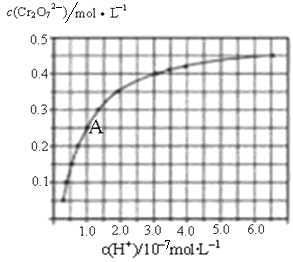
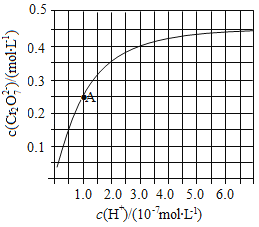
(2)CrO42—和Cr2O72—在溶液中可相互转化。室温下,初始浓度为1.0molL﹣1的Na2CrO4溶液中c(Cr2O72—)随c(H+)的变化如图所示。
 ①用离子方程式表示Na2CrO4溶液中的转化反应 。
①用离子方程式表示Na2CrO4溶液中的转化反应 。
②由图可知,溶液酸性增强,CrO42﹣的平衡转化率 (填“增大“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为 。
(3)用K2CrO4为指示剂,以AgNO3标准液滴定溶液中的Cl﹣,Ag+与CrO42﹣生成砖红色沉淀时到达滴定终点。当溶液中Cl﹣恰好完全沉淀(浓度等于1.0×10﹣5molL﹣1)时,溶液中c (Ag+)为 molL﹣1,此时溶液中c(CrO42﹣)等于 molL﹣1。(Ksp(Ag2CrO4)=2.0×10﹣12、Ksp(AgCl)=2.0×10﹣10)。
(4)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72﹣还原成Cr3+,反应的离子方程式为 。
【答案】(1)溶液蓝紫色变浅,同时产生灰蓝色沉淀,然后沉淀逐渐溶解形成绿色溶液(2分)
(2)①2CrO42-+2H+![]() Cr2O72-+H2O(2分)②增大(2分)1.0×1014(2分)
Cr2O72-+H2O(2分)②增大(2分)1.0×1014(2分)
(3)2.0×10-5(2分)5.0×10-3(2分)
(4)Cr2O72-+3HSO3-+5H+=2Cr3++3SO42-+4H2O(2分)
【解析】
试题分析:(1)Cr(OH)3与Al(OH)3的化学性质相似,可知Cr(OH)3是两性氧化物,能溶解在强碱NaOH溶液中,在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,首先蓝紫色变浅同时产生Cr(OH)3灰蓝色固体,继续滴加,沉淀溶解,Cr(OH)3变为Cr(OH)4-,溶液最终变为绿色。
(2)①随着H+浓度的增大,CrO42-与溶液中的H+发生反应,因此转化为Cr2O72-的离子反应式为:2CrO42- + 2H+![]() Cr2O72- + H2O。
Cr2O72- + H2O。
②根据化学平衡移动原理,溶液酸性增大,c(H+)增大,化学平衡2CrO42-+2H+![]() Cr2O72-+H2O向正反应方向进行,导致CrO42的平衡转化率增大;根据图像可知,在A点时,c(Cr2O72-)=0.25 mol/L,由于开始时c(CrO42)=1.0 mol/L,根据Cr元素守恒可知A点的溶液中CrO42-的浓度c(CrO42)=0.5 mol/L;H+浓度为1.0×10-7 mol/L;此时该转化反应的平衡常数为
Cr2O72-+H2O向正反应方向进行,导致CrO42的平衡转化率增大;根据图像可知,在A点时,c(Cr2O72-)=0.25 mol/L,由于开始时c(CrO42)=1.0 mol/L,根据Cr元素守恒可知A点的溶液中CrO42-的浓度c(CrO42)=0.5 mol/L;H+浓度为1.0×10-7 mol/L;此时该转化反应的平衡常数为![]() ;
;
(3)当溶液中Cl-完全沉淀时,即c(Cl-)=1.0×105 mol·L1,根据溶度积常数Ksp (AgCl)=2.0×1010,可得溶液中c(Ag+)=Ksp(AgCl)/c(Cl-)=2.0×1010÷(1.0×105mol·L1)=2.0×10-5mol·L1;则此时溶液中c(CrO42)=Ksp(Ag2CrO4)/c2(Ag+)=2.0×1012÷(2.0×10-5 )2=5×10-3mol·L1。
(4)NaHSO3具有还原性,Cr2O72具有氧化性,二者会发生氧化还原反应,根据已知条件,结合电子守恒、电荷守恒、原子守恒,可得二者反应的离子方程式为Cr2O72+3HSO3 +5H+==2Cr3++3SO42+4H2O。